题目内容
【题目】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为_________________________。
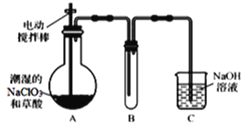
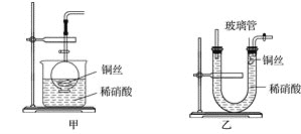
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填字母)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是______________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是__________________________________________________。
②让反应停止的操作方法及原因是_______________________________________________。
(4)以下收集NO气体的装置,合理的是________(填字母)。
a. b.
b.![]() c.
c.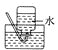 d.
d.![]() e.
e.![]()
【答案】3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑ CD 2NO+O2=2NO2 接收被气体压出U形管的液体,防止稀硝酸溢出 关闭U形管右端导气管上的活塞,反应产生的气体将U形管右端管内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止 cd
【解析】
(1)金属铜可以和稀硝酸之间反应生成硝酸铜、一氧化氮以及水;
(2)①铁、铝的活泼性强于金属铜,会先于金属铜和硝酸之间发生反应;
②NO容易被空气中的氧气氧化为红棕色的NO2气体;
(3)①一氧化氮是难溶于水的气体,生成的气体导致U形管右端气体压强增大,把U形管的液体压入长玻璃管;
②关闭U形管右端导气管上的活塞,反应产生的气体导致U形管右端气体压强增大,将U形管右端内的稀硝酸向下压,使铜丝与稀硝酸分开;
(4)NO能与O2反应,不能用排空气法收集,NO难溶于水,可用排水法收集。
(1)金属铜可以和稀硝酸之间反应生成硝酸铜、一氧化氮以及水,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑;
(2)①实验室若没有铜丝,以铜粒代替铜丝进行实验,包裹铜粒的丝状材料不能是金属铁以及金属铝,因为铁、铝的活泼性强于金属铜,会先于金属铜和硝酸之间发生反应,故答案为:CD;
②试管内有空气,NO容易被空气中的氧气氧化为红棕色的NO2气体,反应的化学方程式为2NO+O2═2NO2;
(3)①一氧化氮是难溶于水的气体,当制取一氧化氮的装置产生一氧化氮气体时,气体难溶于水,生成的气体导致U形管右端气体压强增大,把U形管的液体压入长玻璃管,所以长玻璃管的作用是接收被气体压出U形管的液体,防止稀硝酸溢出,故答案为:接收被气体压出U形管的液体,防止稀硝酸溢出;
②关闭U形管右端导气管上的活塞,反应产生的气体导致U形管右端气体压强增大,将U形管右端内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止,故答案为:关闭U形管右端导气管上的活塞,反应产生的气体将U形管右端管内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止;
(4)NO能与O2反应,不能用排空气法收集,NO难溶于水,可用排水法收集,故cd正确。

 新题型全程检测期末冲刺100分系列答案
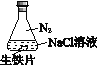
新题型全程检测期末冲刺100分系列答案【题目】研究生铁的锈蚀,下列分析不正确的是
序号 | ① | ② | ③ |
实验 |
|
|
|
现象 | 8小时未观察 到明显锈蚀 | 8小时未观察 到明显锈蚀 | 1小时观察 到明显锈蚀 |
A. ①中,NaCl溶液中溶解的O2不足以使生铁片明显锈蚀
B. ②中,生铁片未明显锈蚀的原因之一是缺少H2O
C. ③中正极反应:O2+4e+ 2H2O ==4OH
D. 对比①②③,说明苯能隔绝O2