题目内容
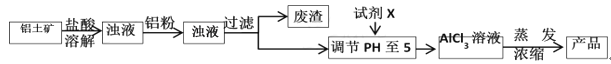
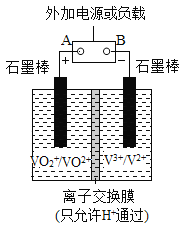
【题目】全钒液流储能电池一次性充电后,续航能力可达1000 km,而充电时间只需3~5 min,被誉为“完美电池”,其原理如图所示(已知V2+呈紫色,V3+呈绿色)。电池放电时,左槽溶液质量增加。下列说法正确的是( )
A. 放电时的正极反应为V3++e-=V2+
B. 放电过程中,右槽溶液由紫色变为绿色
C. 充电时的电流方向由B电极流向A电极
D. 充电时的阴极反应为VO2++2H++e-=VO2++H2O
【答案】B
【解析】
电池放电时,左槽溶液质量增加,由于离子交换膜只允许氢离子通过,则放电时,氢离子向左槽移动,即左槽为正极,正极上发生得电子的还原反应,即VO2++2H++e-═VO2++H2O,右槽为负极,负极发生失电子的氧化反应,即V2+-e-═V3+;充电时,左槽为阳极,VO2+失电子生成VO2+,右槽为阴极,V3+得电子生成V2+,据此分析。
A.放电时,氢离子向左槽移动,即左槽为正极,正极上发生得电子的还原反应,即VO2++2H++e-═VO2++H2O,故A错误;B.放电时,该装置为原电池,左槽作正极,右槽作负极,负极发生失电子的氧化反应,即V2+-e-═V3+,则溶液由紫色变为绿色,故B正确; C.放电时左槽为正极,即A为正极,则充电时A连接电源的正极,B极连接电源的负极,电流由A到B,故C错误;D.充电时,右槽为阴极,阴极上V3+得电子生成V2+,即V3++e-═V2+,故D错误;故答案为B。

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目