题目内容
【题目】将V1mL 1.00mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL),下列叙述正确的是( ) 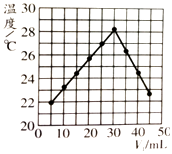
A.实验操作时的环境温度为22℃
B.实验表明热能可转化为化学能
C.该实验表明有水生成的反应都是放热反应
D.NaOH溶液的浓度约为1.50 mol/L
【答案】D
【解析】解:A.从图示观察起始温度即为实验时环境温度,因此该实验开始时温度是20℃,故A错误;B.所以由图示可以看出该反应过程放出热量,表明化学能可能转化为热能,故B错误;
C.只是该反应放热,其他有水生成的反应不一定,如氯化铵和氢氧化钡晶体的反应,故C错误;
D.恰好反应时参加反应的盐酸溶液的体积是30mL,由V1+V2=50ML可知,消耗的氢氧化钠溶液的体积为20mL,
恰好反应时氢氧化钠溶液中溶质的物质的量是n.
HCl+ | NaOH | = | NaCl+H 2O |
1 | 1 | ||
1.0molL﹣1×0.03L | n |
则n=1.0molL﹣1×0.03L=0.03mol,所以浓度是: ![]() =1.5mol/L,故D正确;
=1.5mol/L,故D正确;
故选:D.

练习册系列答案
相关题目