��Ŀ����
����Ŀ����ѧ��Ӧ���ʺ���������������������ء�
��1��ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯����400mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���(�ۼ�ֵ)��
ʱ��(min) | 1 | 2 | 3 | 4 | 5 |
�������(mL)(��״��) | 100 | 240 | 464 | 576 | 620 |
����һʱ��η�Ӧ�������___min(��0~1��1~2��2~3��3~4��4~5)��ԭ����____��
����3~4����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����___(����Һ�������)��
��2����һѧ��Ϊ���Ʒ�Ӧ���ʷ�ֹ��Ӧ�������Բ�������������������������м���������������Һ�Լ�����Ӧ���ʣ�����Ϊ�����е�����________��
A.����ˮ
B.KCl��Һ
C.KNO3��Һ
D.CuSO4��Һ
��3��ij�¶�����4L�ܱ������У�X��Y��Z������̬���ʵ����ʵ�����ʱ��仯������ͼ��
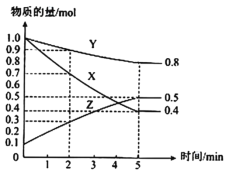
�ٸ÷�Ӧ�Ļ�ѧ����ʽ��___��
�ڸ÷�Ӧ�ﵽƽ��״̬�ı�־��___��
A.X��Y��Z�ķ�Ӧ�������
B.X��Y�ķ�Ӧ���ʱ�Ϊ3��1
C.����������ѹǿ���ֲ���
D.����1molY��ͬʱ����2molZ
��2min��X��ת����Ϊ___��
���𰸡�2~3min ��÷�Ӧ�Ƿ��ȷ�Ӧ����ʱ�¶ȸ�������Ũ�Ƚϴ����Է�Ӧ���ʽϿ� 0.025mol/(L��min) CD 3X(g)+Y(g)![]() 2Z(g) CD 30%
2Z(g) CD 30%
��������
(1)����ͬ�����£���Ӧ����Խ����ͬʱ�����ռ�������Խ�ࣻ�ɱ������ݿ�֪����Ӧ��������ʱ�����2��3 min����Ϊ��Ӧ�Ƿ��ȷ�Ӧ����ʱ�¶ȸ�������Ũ�Ƚϴ����Է�Ӧ���ʽϿ죻�ʴ�Ϊ��2~3min����÷�Ӧ�Ƿ��ȷ�Ӧ����ʱ�¶ȸ�������Ũ�Ƚϴ����Է�Ӧ���ʽϿ죻
��3��4����ʱ��Σ��ռ����������=(576-464)mL=112mL��n(H2)=![]() =0.005mol������������HCl��ϵʽ�����ĵ�n(HCl)=2n(H2)=2��0.005mol=0.01mol����v(HCl)=
=0.005mol������������HCl��ϵʽ�����ĵ�n(HCl)=2n(H2)=2��0.005mol=0.01mol����v(HCl)=![]() =0.025 mol/(Lmin)���ʴ�Ϊ��0.025mol/(L��min)��
=0.025 mol/(Lmin)���ʴ�Ϊ��0.025mol/(L��min)��
��2��A����������ˮ��������Ũ�ȼ�С����Ӧ���ʽ��ͣ���A���У�
B������KCl��Һ��������Ũ�Ƚ��ͣ���Ӧ���ʽ��ͣ���B���У�
C������KNO3��Һ���൱�ں������ᣬ�����Zn��Ӧ����NO��������������C�����У�
D������CuSO4��Һ��Zn��ͭ���ӷ�Ӧ����Cu��Zn��Cu��ϡ���ṹ��ԭ��ض��ӿ췴Ӧ���ʣ���D�����У��ʴ�Ϊ��CD��
��3���ٸ���ͼ֪�����ŷ�Ӧ���У�X��Y�����ʵ������ٶ�Z�����ʵ������ӣ���X��Y�Ƿ�Ӧ���Z���������Ӧ�ﵽƽ��ʱ����n(X)=(1.0-0.4)mol=0.6mol����n(Y)=(1.0-0.8)mol=0.2mol����n(Z)=(0.5-0.1)mol=0.4mol��ͬһ���淴Ӧ��ͬһ��ʱ���ڲμӷ�Ӧ�ĸ����ʵ����ʵ����仯��֮�ȵ��ڻ�ѧ������֮�ȣ�X��Y��Z�Ļ�ѧ������֮��=0.6mol��0.2mol��0.4mol=3��1��2����÷�Ӧ����ʽΪ3X(g)+Y(g)2Z(g)���ʴ�Ϊ��3X(g)+Y(g)![]() 2Z(g)��
2Z(g)��
��A���ò�ͬ���ʱ�ʾ���������棩��Ӧ����֮��ʼ�յ��ڻ�ѧ������֮�ȣ��ﵽƽ��ʱ�ò�ͬ���ʱ�ʾ�������淴Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���A��ѡ��
B�����ŷ�Ӧ�Ľ��У�X��Y�ķ�Ӧ���ʱ�ʼ��Ϊ3��1��������Ϊƽ��״̬�ı�־����B��ѡ��
C���÷�Ӧǰ������ϵ��֮�Ͳ���ȣ�����δƽ��ʱ����������ʵ�����䣬�����ݻ��㶨������ѹǿ��䣬������������ѹǿ���ֲ���ʱ����Ӧ�ﵽƽ��״̬����Cѡ��
D������1molY��ͬʱ����2molZ������1molY�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬����Dѡ��
�ʴ�Ϊ��CD��
��2min��Xת��1.0mol-0.7mol=0.3mol����X��ת����Ϊ![]() ��100%=30%��
��100%=30%��
�ʴ�Ϊ��30%��

����Ŀ��ijͬѧ����ϡ������п��ȡ������ʵ���У����ּ�����������ͭ��Һ�ɼӿ��������������ʡ�
Ϊ�˽�һ���о�����ͭ�������������������ʵ�Ӱ�죬��ͬѧ���������һϵ��ʵ�顣�����������Ļ����Һ�ֱ���뵽6��ʢ�й���Zn���ķ�Ӧƿ�У��ռ����������壬��¼�����ͬ�������������ʱ�䡣����������Һ��������ڻ��ǰ����Һ�����֮�ͣ�
ʵ�� �����Һ | A | B | C | D | E | F |
4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
����CuSO4��Һ/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
��ش��������⣺
������ɴ�ʵ����ƣ����У�V3=___��V8=___��
�ڸ�ͬѧ���ó��Ľ���Ϊ������������CuSO4��Һʱ���������������ʻ�����ߡ����������CuSO4��Һ����һ����ʱ���������������ʷ������½���������������������½�����Ҫԭ��___��
��ʵ��A��ã��ռ�������H2���Ϊ112mL����״���£�ʱ�����ʱ��Ϊ10���ӣ���ѧ��Ӧ������(H2SO4)=___�����Է�Ӧǰ����Һ����仯����