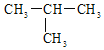��Ŀ����
����Ŀ��������2 L���ݵ������У��ֱ�����ӦA��g��+3B��g��![]() 2C��g����5min���������Ӧ��ƽ��״̬�����м�������A�����ʵ���Ϊ0.4 mol������˵����ȷ���ǣ���
2C��g����5min���������Ӧ��ƽ��״̬�����м�������A�����ʵ���Ϊ0.4 mol������˵����ȷ���ǣ���
��Ӧǰ�����ʵ����ʵ���/mol
A | B | C | |
�� | 1 | 3 | 0 |
�� | 0 | 0 | 2 |
�� | 1.5 | 4.5 | 1 |
A.����5min��C�ķ�Ӧ����Ϊ0.16mol-1��min-1
B.�ﵽƽ��ʱ������A��Ũ���Ǽ��е�2��
C.���з�Ӧ��ƽ�ⳣ�����ڼ��з�Ӧ��ƽ�ⳣ��
D.�ﵽƽ��ʱ���ס�����������C�����ʵ������
���𰸡�D
��������
���õ�Чƽ����з�����
��������ӦA��g��+3B��g��![]() 2C��g��
2C��g��
��ʼ��mol�� 1 3 0
�仯��mol�� 0.6 1.8 1.2
ƽ�⣨mol�� 0.4 1.2 1.2
�������кͼ������ﵽ��ͬƽ��״̬
������A��g��+3B��g��![]() 2C��g��
2C��g��
��ʼ��mol�� 0 0 2
�仯��mol�� 1.2 1.2 0.8
ƽ�⣨mol�� 1.2 1.2 1.2
���������б��дﵽƽ��
A��g��+3B��g��![]() 2C��g��
2C��g��
1.5 4.5 1
��ʼ�����Կ���Ϊ2 6 0���൱�ڼ�������2�����÷�ӦΪ���������С�ķ�Ӧ����ѹǿ����ƽ��������Ӧ������У�
A�����������������ﵽ��ͬ��ƽ��״̬�����ݷ�����֪Ӧ����C�����ʵ���Ϊ0.8mol������5min��C�ķ�Ӧ����Ϊ![]() =0.08mol/(L��min)����A����
=0.08mol/(L��min)����A����
B���������е���ʼ���൱�ڼ�������2�������÷�ӦΪ���������С��ѹǿ����ƽ��������Ӧ������У������A��Ũ�ȱȼ������е�2��С����B����
C����ѧƽ�ⳣ��ֻ���¶ȵ�Ӱ�죬�ͱ������¶���ͬ������ѧƽ�ⳣ�����䣬��C����
D�����������������ﵽƽ��ʱ������������C�����ʵ�����ȣ���D��ȷ��
��ѡD��

 ��У����ϵ�д�
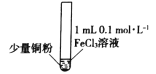
��У����ϵ�д�����Ŀ��ijС��ͬѧͨ��ʵ���о�FeCl3��Һ��Cu�۷�����������ԭ��Ӧ��ʵ���¼���£�
��� | I | II | III |
ʵ�鲽�� |
���������2mL����ˮ |
���������2mL����ˮ |
���������2mL����ˮ |
ʵ������ | ͭ����ʧ����Һ��ɫ��dz����������ˮ������������ | ͭ����ʣ�࣬��Һ��ɫ��ȥ����������ˮ�����ɰ�ɫ���� | ͭ����ʣ�࣬��Һ��ɫ��ȥ�������ɫ����������ˮ���ް�ɫ���� |
����˵������ȷ����
A. ʵ��I��II��III�о��漰Fe3+����ԭ
B. �Ա�ʵ��I��II˵����ɫ�����IJ�����ͭ�۵����й�
C. ʵ��II��III�м�������ˮ��c(Cu2+)��ͬ
D. ��ʵ��III��Ӧ�����Һ�м��뱥��NaCl��Һ���ܳ��ְ�ɫ����
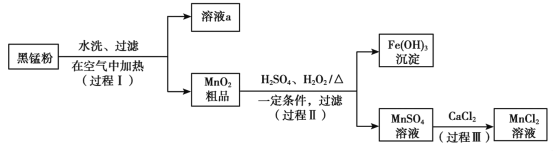
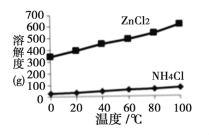
����Ŀ��������������ë֯Ʒ��������±������������ʯӲ������ɫ�����Ը���ĸ��ʯ(��4.5%Cr2O3,����Fe2O3��FeO��MgO��SiO2)Ϊԭ���Ʊ��������Ĺ����������¡�

�±��г�����ؽ������������������������pH:
�������� | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 | Fe(OH)2 |
��ʼ������pH | 2.3 | 8.8 | 4.9 | 7.5 |
������ȫ��pH | 4.1 | 10.4 | 6.8 | 9.7 |
��ش���������:
(1)������ĸ��ʯ�����Ŀ����___________��
(2)Cr2O3��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ________________��
(3)��һ�εμӰ�ˮ����pH��ΧΪ______��
(4)�ڶ��εμӰ�ˮ����pH Ϊ6.8~8.8��Ŀ����___________,Cr(OH)3�� Al(OH)3 һ���������ԣ����ڶ��εμӵİ�ˮ��ΪNaOH��Һ�����ɵ�Cr(OH)3�Ჿ���ܽ⣬д��Cr(OH)3�ܽ�����ӷ���ʽ:___________��