题目内容
16.除杂(括号内为杂质):请把所加试剂和有关离子反应方程式填在空白处.| 试剂 | 离子反应方程式 | |
| ①NaHCO3溶液(Na2CO3) | ||
| ②SiO2(CaCO3) |
分析 ①可通入二氧化碳气体,碳酸钠生成碳酸氢钠;
②CaCO3可与盐酸反应,生成氯化钙、水和二氧化碳气体.
解答 解:①向Na2CO3中通入二氧化碳,会反应生成碳酸氢钠溶液,达到除杂的目的,离子方程式:CO2+H2O+CO32-=2HCO3-;
②碳酸钙与盐酸反应,而二氧化硅不能,则除去SiO2中的CaCO3,选择试剂为稀盐酸,发生的离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:
| . | 试剂 | 离子反应方程式 |
| ①NaHCO3溶液(Na2CO3) | CO2 | CO2+H2O+CO32-=2HCO3- |
| ②SiO2(CaCO3) | 稀盐酸 | CaCO3+2H+=Ca2++CO2↑+H2O |
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,除杂时不能引入新杂质,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列物质在水溶液中存在着电离平衡的是( )
| A. | HF | B. | HNO3 | C. | C2H5OH(酒精) | D. | Na2SO4 |
4.下列说法正确的是( )
| A. | 乙烯和聚乙烯都可以发生加成反应 | |
| B. | 甲苯分子中的所有碳原子共平面,聚乙烯分子中的所有碳原子共直线 | |
| C. | 乙酸乙酯、油脂分别在NaOH溶液中反应都有醇生成 | |
| D. | Ba2+中毒,可以吃煮熟的鸡蛋解毒 |
11.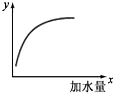 如图表示 25℃时,向0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
如图表示 25℃时,向0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
 如图表示 25℃时,向0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
如图表示 25℃时,向0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )| A. | c(H+) | B. | HA的电离平衡常数Ka | ||
| C. | $\frac{c({H}^{+})}{c(HA)}$ | D. | 水的离子积常数Kw |
1.人们在禽流感疫区通常洒石灰进行消灭病毒,甚至是低矮树木的叶子上都洒上了石灰,效果较好.根据有关化学知识,判断下列说法错误的是( )
| A. | 由于生石灰与水产生的氢氧化钙显碱性,可以使病毒蛋白失去活性 | |
| B. | 饱和石灰水中加入生石灰,在温度不变的情况下,pH不变 | |
| C. | 饱和石灰水中加入生石灰,在温度不变的情况下,溶液中Ca2+的物质的量不变 | |
| D. | 给饱和石灰水溶液升高温度,c(OH-)的浓度降低 |
8.下列物质中,属于天然高分子化合物的是( )
| A. | 羊毛 | B. | 绦纶 | C. | 丁苯橡胶 | D. | 锦纶 |
7.已知甲苯的一氯代物有4种,则甲苯完全氢化后的一氯代物有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
 ,C
,C ,D
,D ,F
,F ,E
,E ;
;