题目内容
11.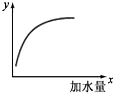 如图表示 25℃时,向0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
如图表示 25℃时,向0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )| A. | c(H+) | B. | HA的电离平衡常数Ka | ||
| C. | $\frac{c({H}^{+})}{c(HA)}$ | D. | 水的离子积常数Kw |
分析 根据图象可知,加入水稀释过程中,纵坐标y的数值逐渐增大,
A.弱酸溶液在稀释过程中溶液中氢离子浓度减小;
B.电离平衡常数与温度有关,温度不变,电离平衡常数不变;
C.稀释过程中HA分子的物质的量逐渐减小,氢离子的物质的量逐渐增大,则该比值增大;
D.水的离子积只受温度的影响.
解答 解:根据图象可知,加入水稀释HA的过程中,纵坐标y会逐渐增大,
A.稀释HA溶液的过程中,溶液中的氢离子的物质的量浓度会逐渐减小,故A错误;
B.HA的电离平衡常数Ka只受温度影响,与加入水的量无关,故B错误;
C.稀释过程中HA分子的物质的量逐渐减小,氢离子的物质的量逐渐增大,在同一溶液中,则该比值会逐渐增大,与图象变化一致,故C正确;
D.水的离子积与温度有关,加入水的过程中水的离子积不变,故D错误;
故选C.
点评 本题考查了弱电解质的电离平衡及其影响因素,题目难度中等,注意掌握影响弱电解质电离的因素,明确水的离子积、弱电解质的电离平衡常数只受温度影响.

练习册系列答案
 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
1.己烷雌酚的一种合成路线如下:
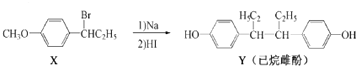
下列叙述正确的是( )

下列叙述正确的是( )
| A. | 在NaOH水溶液中加热,化合物X可发生消去反应 | |
| B. | 化合物Y不能与HCHO发生反应 | |
| C. | 用FeCl3溶液可鉴别化合物X和Y | |
| D. | 化合物Y中共含有四种氢原子 |
19.下列说法正确的是( )
| A. | 1-丁烯、2-丁烯都存在顺反异构 | |
| B. | 乙二醇和丙三醇为同系物 | |
| C. | 正戊烷、异戊烷、新戊烷的沸点逐渐降低 | |
| D. | 淀粉、纤维、脂肪、蛋白质都是天然高分子化合物 |
16.除杂(括号内为杂质):请把所加试剂和有关离子反应方程式填在空白处.
| 试剂 | 离子反应方程式 | |
| ①NaHCO3溶液(Na2CO3) | ||
| ②SiO2(CaCO3) |
3.信息、材料和能源被称为新科技革命的三大支柱.下列说法错误的是( )
| A. | 目前中美日等国掌握的陶瓷发动机技术,大大提高了发动机的能量转化效率 | |
| B. | 在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源 | |
| C. | 合成高分子材料的广泛应用是有百利而无一害的 | |
| D. | 2013年6月11日发射成功的“神舟十号”载人飞船使用了大量的复合材料 |
20.市场上常用的一种锂离子电池的电池反应式为:Li+2Li0.35NiO2$?_{充电}^{放电}$2Li0.85NiO2,下列说法中不正确的是( )
| A. | 该电池不能用水溶液作为电解质 | |
| B. | 放电时,Li+向负极移动 | |
| C. | 充电时,电极Li0.85NiO2质量会减小 | |
| D. | 放电时,负极的反应为:Li-e-═Li+ |
2.木糖醇是一种新型的甜味剂,它具有甜味足、溶解性好、防龋齿、适合糖尿病患者的需要.它是一种白色粉末状的结晶,结构简式为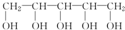 ,下列有关木糖醇的叙述中不正确的是( )
,下列有关木糖醇的叙述中不正确的是( )
 ,下列有关木糖醇的叙述中不正确的是( )
,下列有关木糖醇的叙述中不正确的是( )| A. | 木糖醇是一种单糖,与葡萄糖互为同系物 | |
| B. | 1 mol木糖醇与足量钠反应最多可产生2.5 mol H2 | |
| C. | 木糖醇易溶于水,能发生酯化反应 | |
| D. | 糖尿病患者可以食用 |
