题目内容
5.(CH3)2CHCH2OH是某有机物的加氢还原产物,该有机物可能是( )| A. | 乙醛的同系物 | B. | 丙醛的同分异构体 | ||
| C. | CH2=C(CH3)CHO | D. | CH3CH2COCH3 |
分析 有机物加氢反应后的还原产物是CH3CH(CH3)CH2OH,则有机物中含有不饱和键,
A、醛加氢还原可以得到醇:CH3CH(CH3)CHO+H2→CH3CH(CH3)CH2OH;
B、丙醛的同分异构体为丙酮,加成反应得到2-丙醇;
C、烯醛加氢还原可以得到醇:CH2=C(CH3)CHO+2H2→CH3CH(CH3)CH2OH;
D、CH3CH2COCH3 和氢气加成得到2-丁醇,CH3CH2CH(OH)CH3;
解答 解:A、只加成双键就是异丁醛,烃基部分为C3H7,比乙醛的烃基部分多2个CH2,符合同系物的条件,故A正确;
B、题给需要4个碳,而丙醛的同分异构体只能给3个,丙醛的同分异构体为丙酮,加成反应得到2-丙醇,故B错误;
C、CH2=C(CH3)CHO中双键加成,醛基被还原为醇羟基,CH2=C(CH3)CHO+2H2→CH3CH(CH3)CH2OH,故C正确;
D、酮加氢还原的产物是仲醇,而题给是伯醇,加成反应得到是2-丁醇,CH3CH2CH(OH)CH3,故D错误;
故选AC.
点评 丙酮考查了加成反应和醇结构的分析,同系物的结构理解应用,注意碳碳双键、醛基、羰基都可以和氢气发生加成反应形成羟基,题目难度中等.

练习册系列答案
相关题目
15. 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:
回答下列问题:
(1)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.Na2CO3 c.NaClO
pH由小到大排列的顺序是a<c<b(用编号填写).
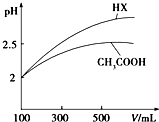
(2)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数大于(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数.稀释后,HX溶液中水电离出来的C(H+)大于(填“大于”、“小于”或“等于”)醋酸溶液中水电离出来的C(H+).
 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.Na2CO3 c.NaClO
pH由小到大排列的顺序是a<c<b(用编号填写).
(2)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数大于(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数.稀释后,HX溶液中水电离出来的C(H+)大于(填“大于”、“小于”或“等于”)醋酸溶液中水电离出来的C(H+).
10.某溶液中含有HCO3-,CO32-,SO32-,CH3COO-,SO42-等五种离子,若向其中加入Na2O2粉末充分反应后(溶液体积变化忽略不计),溶液中离子浓度基本保持不变的是( )
| A. | CH3COO- | B. | SO42-,CO32- | C. | CH3COO-SO42- | D. | SO42- |
14.用CH4催化还原 NOx可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ•mol-1
下列说法不正确的是( )
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ•mol-1
下列说法不正确的是( )
| A. | 由反应 ①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O (l)△H>-574 kJ•mol-1 | |
| B. | 反应 ①②转移的电子数相同 | |
| C. | 若用标准状况下4.48LCH4还原NO2至N2,放出的热量为173.4kJ | |
| D. | 若用标准状况下4.48LCH4还原 NO2至 N2,整个过程中转移的电子总数为1.60 mol |
15.下列指定物质的所占有体积约为最大的是( )
| A. | 标准状况下56g铁原子 | B. | 20℃、101kPa时36.5gHCl | ||
| C. | 标准状况下6.02×1023个NH3 | D. | 标准状况下1molC2H5OH |

 实验室通常用浓硫酸和乙醇反应来制取乙烯,常因温度过高而生成少量的二氧化硫.有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫,试回答下列问题.
实验室通常用浓硫酸和乙醇反应来制取乙烯,常因温度过高而生成少量的二氧化硫.有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫,试回答下列问题.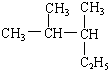 2,3-二甲基戊烷
2,3-二甲基戊烷 .
.