题目内容
14.用CH4催化还原 NOx可以消除氮氧化物的污染.例如:①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ•mol-1
下列说法不正确的是( )
| A. | 由反应 ①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O (l)△H>-574 kJ•mol-1 | |
| B. | 反应 ①②转移的电子数相同 | |
| C. | 若用标准状况下4.48LCH4还原NO2至N2,放出的热量为173.4kJ | |
| D. | 若用标准状况下4.48LCH4还原 NO2至 N2,整个过程中转移的电子总数为1.60 mol |
分析 A.气态水变为液态水要放出热量,导致其焓变小于0;
B.反应①中C元素化合价由-4价变为+4价、N元素化合价由+4价变为+2价,转移电子数为8;反应②中C元素化合价由-4价变为+4价、N元素化合价由+2价变为0价,转移电子数为8;
C.标况下n(CH4)=$\frac{4.48L}{22.4L/mol}$=0.2mol,将方程式①+②得2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O(g);△H=-1734kJ•mol-1,根据甲烷和反应热之间关系式计算;
D.标况下n(CH4)=$\frac{4.48L}{22.4L/mol}$=0.2mol,将方程式①+②得2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O(g);△H=-1734kJ•mol-1,该反应中转移电子数为16,根据甲烷和转移电子之间关系式计算.
解答 解:A.气态水变为液态水要放出热量,导致其焓变小于0,所以由反应 ①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O (l)△H<-574 kJ•mol-1,故A错误;
B.反应①中C元素化合价由-4价变为+4价、N元素化合价由+4价变为+2价,转移电子数为8;反应②中C元素化合价由-4价变为+4价、N元素化合价由+2价变为0价,转移电子数为8,所以反应 ①②转移的电子数相同,故B正确;
C.标况下n(CH4)=$\frac{4.48L}{22.4L/mol}$=0.2mol,将方程式①+②得2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O(g);△H=-1734kJ•mol-1,根据甲烷和反应热之间关系式得放出热量=$\frac{0.2mol}{2}×1734kJ$=173.4kJ,故C正确;
D.标况下n(CH4)=$\frac{4.48L}{22.4L/mol}$=0.2mol,将方程式①+②得2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O(g);△H=-1734kJ•mol-1,该反应中转移电子数为16,根据甲烷和转移电子之间关系式得转移电子物质的量=$\frac{16mol}{2mol}×0.2mol$=1.60mol,故D正确;
故选A.
点评 本题以热化学反应方程式为载体考查盖斯定律、反应热的有关计算等知识点,侧重考查学生分析计算能力,易错选项是A,注意放热反应焓变小于0,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| 选项 | 理由 | 结论 |
| A | 相同物质的量浓度溶液的pH: Ca(ClO)2>CH3COONa | 酸性:CH3COOH>HClO |
| B | 同体积相同pH的盐酸和醋酸与相同的锌 反应的速率:醋酸>盐酸 | 酸性:HCl>CH3COOH |
| C | 相同条件下的沸点: H2O>NH3 | 非金属性:O>N |
| D | 相同物质的量得到电子的数目: 稀硝酸>浓硝酸 | 氧化性:稀硝酸>浓硝酸 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 乙醛的同系物 | B. | 丙醛的同分异构体 | ||
| C. | CH2=C(CH3)CHO | D. | CH3CH2COCH3 |
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol N2、3mol H2 | 4mol NH3 |
| NH3的浓度(mol•L-1) | c1 | c2 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ |
| 气体密度 | ρ1 | ρ2 |
| 反应物转化率 | α1 | α2 |
| A. | c1<c2<2c1 | B. | a+b>92.4 | C. | α1+α 2=1 | D. | ρ2=3ρ1 |
| A. | $\frac{3n}{2a}$ mol/L | B. | $\frac{2n}{3a}$ mol/L | C. | $\frac{2n}{a}$mol/L | D. | $\frac{3n}{a}$mol/L |
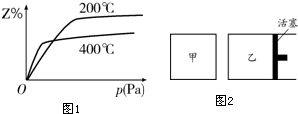
 某实验兴趣小组利用如图所示装置进行电解食盐水并检验其生成产物的实验,当图中开关k闭合片刻后,试填空:
某实验兴趣小组利用如图所示装置进行电解食盐水并检验其生成产物的实验,当图中开关k闭合片刻后,试填空:
 名称是3,5-二甲基庚烷.
名称是3,5-二甲基庚烷.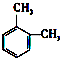 名称是1,2-二甲苯.
名称是1,2-二甲苯.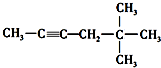 名称是5,5-二甲基-2-己炔.
名称是5,5-二甲基-2-己炔. 名称是4-甲基-1-戊烯.
名称是4-甲基-1-戊烯.