题目内容
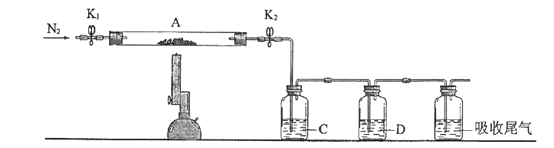
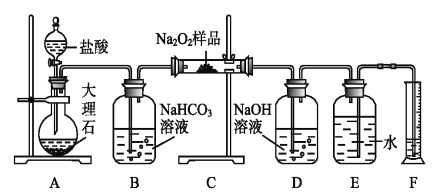
【题目】由两种元素组成的矿物A,测定A的组成及制取化合物D的流程如图:

请回答:
(1)A的化学式为______
(2)写出③的离子方程式:______
(3)写出D溶于足量稀硝酸的化学方程式:______
【答案】Cu2S SO2+2Fe3++2H2O=2Fe2++SO42-+4H+ 3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O
【解析】
由两种元素组成的矿物 A,与氧气在高温下得到黑色B、无色气体C,B在高温下反应生成砖红色沉淀D,则B为CuO,D为Cu2O.无色气体C与氯化铁溶液反应得到E,E你同意氯化钡反应得到白色沉淀F,则C为SO2、E为Fe2(SO4)3、F为BaSO4,则A中含有Cu、S两种元素,由S原子守恒:n(S)=n(SO2)=n(BaSO4)=0.01mol,1.6gA中Cu原子物质的量为0.02mol,A中Cu、S原子的物质的量之比=0.02mol:0.01mol=2:1,所以A的化学式为Cu2S,以此解答该题。
(1)由以上分析可知A为Cu2S,故答案为:Cu2S;
(2)③的离子方程式为SO2+2Fe3++2H2O=2Fe2++SO42-+4H+;
(3)D为Cu2O,溶于足量稀硝酸的化学方程式为3Cu2O+14HNO3 =6Cu(NO3)2 +2NO+7H2O。

【题目】氯化亚铜常用作有机合成工业中的催化剂,为白色晶体,不溶于乙醇,微溶于水, 易溶于浓盐酸形成络合离子([CuCl2]-)。受潮露置空气中迅速氧化成碱式盐。实验室 用 下列流程制备:
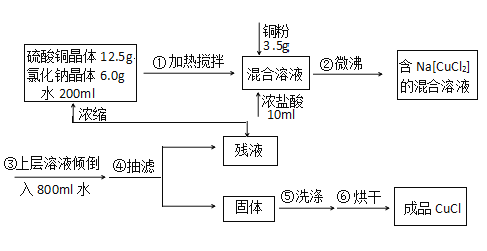
注:Na[CuCl2](易电离,溶液无色)水NaCl+CuCl↓(白色沉淀)。请回答:
(1)写出实验室制取Na[CuCl2]的离子方程式_____________。
(2)判断步骤②反应完全的现象是_______________。
(3)步骤④有关抽滤操作,下列说法正确的是_________。
A. 选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B. 在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的长导管相接
C. 抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D. 洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(4)步骤⑤用乙醇的水溶液洗涤的目的是______________。
(5)步骤⑥烘干须在真空干燥箱中进行,其原因是___________________。
(6)氯化亚铜的定量
①取样品0.25g和10ml过量的FeCl3溶液于250ml锥形瓶中,充分溶解。
②用0.10mol·L-1硫酸锶铈[Ce(SO4)2]标准溶液滴定。
已知:CuCl+FeCl3=CuCl2+FeCl2; Fe2++Ce4+=Fe3++Ce3+
三次平行试验结果如下(平行试验结果相差不能超过1%):
平行试验次数 | 1 | 2 | 3 |
0.25g样品消耗硫酸铈标准溶液的体积(ml) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为____________。(结果保留三位有效数字)