题目内容
【题目】利用化学反应可以为人类提供能源,也可用来解决环境问题。
(1)已知某些化学键的键能数据如下:
化学键 | H-H | O=O | O-H |
键能kJ·mol-1 | 436 | 495 | 463 |
①写出H2与O2反应生成水蒸气的热化学方程式____________;
②利用该反应设计成燃料电池,已知该电池每发1kW·h电能生成360g水蒸气,则该电池的能量转化率为_____%(结果保留三位有效数字)。
(2)三室式电渗析法可以处理含K2SO4的废水,原理如图所示,两极均为惰性电极,ab为阳离子交换膜,cd为阴离子交换膜。

①阴极区的pH______(填“升高”或“降低”);
②阳极发生的电极反应式为__________;
③当电路中通过1mol电子的电量时,阴极上生成气体的体积为_____L(标准状况)。
【答案】 2H2(g)+O2(g)===2H2O(g) △H =-485kJ·mol-1 74.2 升高 4OH--4e-===2H2O+O2↑(或 2H2O-4e-=== O2↑+4H+) 11.2
【解析】(1)①反应热等于反应物的键能总和减去生成物的键能总和;
②电池的能量转化率为=实际产生的热量/理论产生的热量×100%;
(2)三室式电解含K2SO4的废水,两极均为惰性电极,阳极水电离出的氢氧根离子放电,生成氧气和氢离子,阴极水电离出的氢离子放电生成氢气和氢氧根离子。
(1)①反应热等于反应物的键能总和减去生成物的键能总和,因此,反应热是436 kJ·mol-1×2+495 kJ·mol-1-463 kJ·mol-1×4=-485kJ·mol-1,所以H2与O2反应生成水蒸气的热化学方程式为:2H2(g)+O2(g)===2H2O(g) △H =-485kJ·mol-1 ,
答案为:2H2(g)+O2(g)===2H2O(g) △H =-485kJ·mol-1 ;
②1度电的能量为3600kJ,按照反应的化学方程式的化学能量的计算,每生成2mol水蒸气放出485 kJ的热量,则生成360g水蒸气放出热量=485 kJ×![]() =4850 kJ,
=4850 kJ,
能量转化率为:![]() 100%=74.2%,
100%=74.2%,
答案为:74.2;
(2)①阴极氢离子放电生成氢气和氢氧根离子,阴极区的pH升高;
②阳极氢氧根离子放电,生成氧气和氢离子,阳极发生的电极反应式为4OH--4e-===2H2O+O2↑(或 2H2O-4e-=== O2↑+4H+);
③当电路中通过1mol电子的电量时,阴极会有0.5molH2生成,阴极上生成气体标况下体积为11.2L。
答案为:升高 ;4OH--4e-===2H2O+O2↑(或 2H2O-4e-=== O2↑+4H+); 11.2。

 阅读快车系列答案
阅读快车系列答案【题目】碘及其化合物主要用于医药、照相及染料等。碘是合成碘化物的基本原料。
(一) 实验室测定KI溶液中I-的含量
量取25.00mLKI溶液溶液于250mL锥形瓶中,分别加入少量稀H2SO4和稍过量的NH4Fe(SO4)2·12H2O溶液,摇匀。小火加热蒸发至碘完全升华,取下锥形瓶冷却后,加入稀H2SO4,再加入几滴二苯胺磺酸钠(用作指示剂,被强氧化剂氧化为紫色),用0.0250mol·L-1标准K2Cr2O7溶液进行滴定至终点。重复3次,平均每次消耗K2Cr2O7溶液20.00mL(已知反应:①2Fe3++2I-=2Fe2++I2 ②6Fe2++Cr2O72-+14H+==6Fe3++2Cr3++7H2O
(1)在滴定过程中,下列操作(其他操作正确)会造成测定结果有误差的是_________________。
A.终点读数时俯视读数,滴定前平视读数
B.锥形瓶水洗后未干燥
C.滴定管未用标准K2Cr2O7溶液润洗
D.盛标准K2Cr2O7溶液的滴定管,滴定前有气泡,滴定后无气泡
(2)该实验达到滴定终点时,现象为__________________。
(3)根据滴定有关数据,该KI溶液中I-含量是________g·L-1。
(二) 某实验小组认为氧气可以氧化KI 溶液中的I-,其做了下列实验探究影响该反应的因素。
实验 | 气体a | 编号及现象 |
| 空气(含HCl) | Ⅰ.溶液迅速呈黄色 |
空气(含CO2) | Ⅱ.长时间后,溶液呈很浅的黄色 | |
空气 | Ⅲ.长时间后,溶液无明显变化 |
(4)装置A (含导管)的名称为_________________。
(5)通入a为空气(含HCl)时,发生反应的离子方程式为______________________。
(6)实验Ⅲ的作用是________________________。
(7)用CCl4萃取Ⅰ、Ⅱ、Ⅲ的溶液,萃取后下层溶液的颜色均无色。取萃取后上层溶液,用淀粉检验:Ⅰ、Ⅱ的溶液变蓝;Ⅲ的溶液未变蓝。溶液变蓝说明Ⅰ、Ⅱ中生成了__________________________。
(8)查阅资料: I2易溶于KI 溶液。下列实验证实了该结论并解释Ⅰ、Ⅱ的萃取现象。

现象X是_____。用KI萃取Ⅰ、Ⅱ的溶液,萃取后下层溶液颜色均无色的原因是_________________。
(9)综合实验证据说明影响I-被氧化的因素及对应关系:__________________________。
【题目】减少二氧化碳的排放,氮氧化物、二氧化硫的处理与利用是一项重要的热点课题.
(1)Ⅰ.CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)C2H4(g)+4H2O(g)△H 在0.1MPa时,按n(CO2):n(H2)=1:3投料,图1所示不同温度(T)下,平衡时的四种气态物质的物质的量(n)的关系. 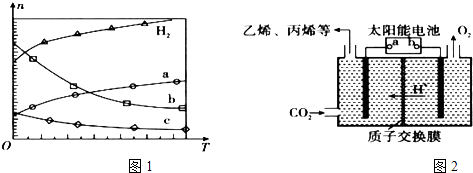
①该反应的△H0(填“>”、“=”或“<”).
②曲线b表示的物质为 .
③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是 .
(2)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如图2所示. b为电源的极,电解时,生成乙烯的电极反应式是 .
(3)Ⅱ.用活性炭还原法可以处理氮氧化物.如反应:C(s)+2NO(g)N2(g)+CO2(g)△H=Q kJmol﹣1 . 在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①T1℃时,该反应的平衡常数K= .
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是(答一种即可).
(4)Ⅲ.工业上可以用NaOH溶液或氨水吸收过量的SO2 , 分别生成NaHSO3、NH4HSO3 , 其水溶液均呈酸性.相同条件下,同浓度的两种酸式盐的水溶液中c(SO32﹣)较小的是 , 用文字和化学用语解释原因 .

