题目内容
【题目】下列实验方案不能达到目的的是
A. 用裂化汽油萃取碘水中的碘
B. 用水鉴别苯、四氯化碳、乙醇三种无色液体
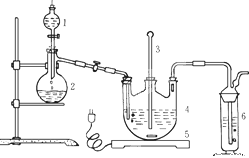
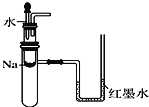
C. 用如图装置验证Na和水反应是否为放热反应
D. 往酸性KMnO4溶液中加入乙醇,验证乙醇的还原性
【答案】A
【解析】A、因为裂化汽油中含有不饱和分子,如烯烃等,会和碘发生加成反应, 不能用裂化汽油萃取碘水中的碘,选项A选;B、碘易溶于苯和四氯化碳,苯的密度比水小,有颜色的液体在上层,四氯化碳的密度比水大,有颜色液体在下层,碘水与乙醇互溶,液体不分层,选项B不选;C、放热,气体热胀冷缩,图U型管中水柱左高右低,说明反应放热,选项C不选;D、因高锰酸钾具有强氧化性,则往酸性KMnO4溶液中加入乙醇,溶液褪色,验证乙醇具有还原性,选项D不选;答案选A。

【题目】研究物质的微观结构,有助于人们理解物质变化的本质。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
电离能 | I1 | I2 | I3 | I4 | I5 | …… |
Im/kJ·mol-1 | 578 | 1817 | 2745 | 11575 | 14830 | …… |
则该元素是______(填元素符号)。
(2)氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
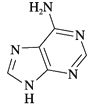
①维生素B4结构如图所示,则碳原子的轨道杂化类型是_________;1 mol维生素B4分子中含有σ键的数目为________。
②NF3的空间构型为______(用文字描述);与NF3分子互为等电子体的阴离子为______(填化学式)。
(3)过渡元素常与H2O、NH3、CN-、SCN-等形成配合物。
①C、N、O三种元素的电负性由大到小的顺序为________。
②X、Y均为第四周期元素。X基态原子的内层轨道全部排满电子,且最外层电子数为1。Y基态原子在同周期元素中未成对电子数最多,则X+基态核外电子排布式________;元素Y在周期表中位于第________族。
③在配离子[Fe(SCN)]2+中,提供空轨道的是________;[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,则[Zn(CN)4]2-的结构可用示意图表示为________。