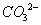题目内容
列各组离子一定能在指定环境中大量共存的是( )
A.在c(H+)=10-10 mol/L的溶液中 Al3+、NH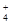 、Cl- 、NO 、Cl- 、NO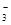 |
B.pH值为13的溶液 K+ 、SO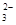 、Na+、S2- 、Na+、S2- |
| C.水电离出来的c(H+)=10-12mol/L的溶液 K+、NH4+、Cl-、ClO- |
D.甲基橙呈红色的溶液中 Fe3+、Na+ 、SO42-、CO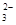 |
B
试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A中溶液显碱性,则Al3+、NH4+不能大量共存;B中溶液也是显碱性的,可以大量共存;C中水的电离是被抑制的,则溶液可能显酸性,也可能显碱性。如果显酸性,则ClO-不能大量共存,如果显碱性,NH4+不能大量共存;D中使甲基橙呈红色的溶液显酸性,则CO32-不能大量共存,且Fe3+和CO32-本身之间也不能大量共存,答案选B。
点评:该题是高考中的高频题,属于中等难度的试题,侧重对学生基础知识的训练和检验。有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。该题需要明确离子不能大量共存的一般情况,即(1)能发生复分解反应的离子之间;(2)能生成难溶物的离子之间;(3)能发生氧化还原反应的离子之间;(4)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有:(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”共存等。

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
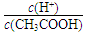 将变小
将变小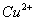 、
、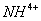 、
、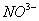 、
、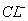
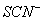 、
、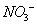 、
、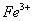 、
、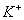
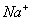 、
、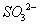
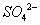 、
、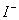 、
、