题目内容
从下列事实所得出的结论或给出的解释正确的是
| | 实验事实 | 结论或解释 |
| A | 将40 g NaOH溶于1 L蒸馏水中 | 该溶液的物质的量浓度为1mol﹒L-1 |
| B | 0.1 mol/L CH3COOH溶液在稀释过程中 | 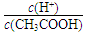 将变小 将变小 |
| C | 酸H2X为弱酸 | 常温下,盐NaHX溶液pH一定大于7 |
| D | 在溶液的稀释过程中 | 离子浓度:有的可能增大,有的可能减小,有的可能不变 |
D
试题分析:A不正确,因为不能确定溶液的体积;醋酸是弱电解质,稀释促进电离。则稀释过程中氢离子的物质的量增加,醋酸分子的物质的量减少,所以
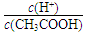 将变大,B不正确;C不正确,如果HX-的电离程度大于水解程度,溶液显酸性;因此正确的答案选D。
将变大,B不正确;C不正确,如果HX-的电离程度大于水解程度,溶液显酸性;因此正确的答案选D。点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力的培养,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和抽象思维能力,提高学生的学习效率和应试能力。

练习册系列答案
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
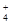 、Cl- 、NO
、Cl- 、NO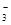
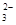 、Na+、S2-
、Na+、S2-