题目内容
如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的,这个规律称为盖斯定律.据此回答下列问题:
(1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
丙烷脱氢可得丙烯.
已知:C3H8(g)-→CH4(g)+HCCH(g)+H2(g)△H1=+156.6kJ?mol-1
CH3CH═CH2(g)-→CH4(g)+HCCH(g)△H2=+32.4kJ?mol-1
则相同条件下,丙烷脱氢得丙烯的热化学方程式为 .
(2)已知:Na2CO3?10H2O(s)═Na2CO3(s)+10H2O(g)△H1=+532.36kJ?mol-1
Na2CO3?10H2O(s)═Na2CO3?H2O(s)+9H2O(g)△H2=+473.63kJ?mol-1
写出Na2CO3?H2O(s)脱水反应的热化学方程式 .
(1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
丙烷脱氢可得丙烯.
已知:C3H8(g)-→CH4(g)+HCCH(g)+H2(g)△H1=+156.6kJ?mol-1
CH3CH═CH2(g)-→CH4(g)+HCCH(g)△H2=+32.4kJ?mol-1
则相同条件下,丙烷脱氢得丙烯的热化学方程式为
(2)已知:Na2CO3?10H2O(s)═Na2CO3(s)+10H2O(g)△H1=+532.36kJ?mol-1
Na2CO3?10H2O(s)═Na2CO3?H2O(s)+9H2O(g)△H2=+473.63kJ?mol-1
写出Na2CO3?H2O(s)脱水反应的热化学方程式
考点:热化学方程式,用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:(1)依据题中热化学方程式和盖斯定律写出丙烷脱氢得丙烯的热化学方程式;
(2)依据热化学方程式和盖斯定律进行计算写出Na2CO3?H2O(s)脱水反应的热化学方程式.
(2)依据热化学方程式和盖斯定律进行计算写出Na2CO3?H2O(s)脱水反应的热化学方程式.
解答:
解:(1)①C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ?mol-1
②CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=+32.4kJ?mol-1
依据盖斯定律①-②可得:C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ/mol,
故答案为:C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ/mol;
(2)①Na2CO3?10H2O(s)═Na2CO3(s)+10H2O(g)△H1=+532.36kJ?mol-1,
②Na2CO3?10H2O(s)═Na2CO3?H2O(s)+9H2O(g)△H2=+473.63kJ?mol-1,
由盖斯定律①-②可得:Na2CO3?H2O(s)═Na2CO3(s)+H2O(g)△H=+58.73kJ?mol-1,
故答案为:Na2CO3?H2O(s)═Na2CO3(s)+H2O(g)△H=+58.73kJ?mol-1.
②CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=+32.4kJ?mol-1
依据盖斯定律①-②可得:C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ/mol,
故答案为:C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ/mol;
(2)①Na2CO3?10H2O(s)═Na2CO3(s)+10H2O(g)△H1=+532.36kJ?mol-1,
②Na2CO3?10H2O(s)═Na2CO3?H2O(s)+9H2O(g)△H2=+473.63kJ?mol-1,
由盖斯定律①-②可得:Na2CO3?H2O(s)═Na2CO3(s)+H2O(g)△H=+58.73kJ?mol-1,
故答案为:Na2CO3?H2O(s)═Na2CO3(s)+H2O(g)△H=+58.73kJ?mol-1.
点评:本题考查了盖斯定律的应用、热化学方程式的书写,题目难度中等,注意掌握热化学方程式的书写原则,明确盖斯定律的含义,能够根据盖斯定律写出热化学方程式.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
下列反应离子方程式表示不正确的是( )
| A、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
| B、Fe3O4与稀HNO3反应:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C、向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| D、向次氯酸钠溶液中通入少量SO2:ClO-+SO2+H2O=Cl-+SO42-+2H+ |
下列各组离子在给定条件下能大量共存的是( )
| A、能使pH试纸呈红色的溶液:Na+、NH4+、Cl-、NO3- |
| B、滴入KSCN溶液显血红色的溶液:K+、Na+、CO32-、I- |
| C、能与铝反应产生H2的溶液:K+、Fe2+、Cl-、NO3- |
| D、常温下由水电离出的c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl- |
下列相关表达正确的是( )
| A、亚硫酸的电离方程式:H2SO3=2H++SO2-3 | ||
B、中子数为18的氯原子的原子符号:
| ||
| C、(CH3)2CHCH2CH2OH的名称:3-甲基-1-丁醇 | ||
D、HOCH2COOH缩聚产物的结构简式: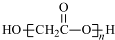 |
 (1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O.已知室温下2g SiH4自燃放出热量89.2kJ.SiH4自燃的热化学方程式为
(1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O.已知室温下2g SiH4自燃放出热量89.2kJ.SiH4自燃的热化学方程式为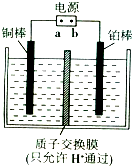 工业上将烟气中的二氧化硫转化为硫,常用的两种方法分别是热解气还原法和离子膜电解法.
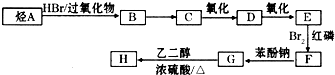
工业上将烟气中的二氧化硫转化为硫,常用的两种方法分别是热解气还原法和离子膜电解法. )可由下列路线合成:
)可由下列路线合成: