题目内容
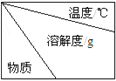
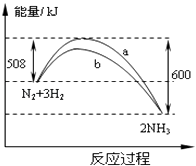
【题目】在一定温度下,将冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.
请回答下列问题:
(1)“O”点冰醋酸不能导电的原因是 .
(2)a、b、c三点对应的溶液中,C(H+)由小到大的顺序为 . (填字母,后同)
(3)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是 .
(4)a、b、c三点对应的溶液中,水的电离程度最大的是 .
(5)若使c点对应的溶液中的c(CH3COO﹣)增大,在下列措施中,可行的是 (填字母,后同).
A.加热
B.加KOH固体
C.加水
D.加CH3COONa固体
E.加锌粒
(6)在稀释过程中,随着醋酸浓度的降低,下列各量始终保持增大趋势的是 .
A.C(H+)
B.H+物质的量
C.C(OH﹣)
D.![]() .
.
【答案】
(1)无自由移动的离子
(2)cab
(3)c
(4)c
(5)A,B,D,E
(6)B,D
【解析】解:(1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强,冰醋酸中没有自由移动的离子,所以冰醋酸不导电,
故答案为:无自由移动的离子;
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为b<a<c,氢离子浓度由小到大的顺序为cab,
故答案为:cab;
(3)溶液越稀,越促进醋酸电离,CH3COOH的电离程度最大的是c,
故答案为:c;
(4)溶液中氢离子浓度越小,对水的电离抑制程度越小,c点氢离子浓度最小,水的电离程度最大,
故答案为:c;
(5)要使醋酸根离子浓度增大,可以采用加热、加入含有醋酸根离子的物质、加入和氢离子反应的物质,
A.加热促进醋酸电离,则溶液中醋酸根离子浓度增大,故正确;
B.加NaOH固体,氢氧化钠和氢离子反应促进醋酸电离,所以醋酸根离子浓度增大,故正确;
C.加水稀释能促进醋酸电离,但醋酸根离子浓度减小,故错误;
D.加固体CH3COONa,能抑制醋酸电离,但醋酸钠电离出的醋酸根离子大于抑制醋酸电离出的醋酸根离子,所以醋酸根离子浓度增大,故正确;
E.加入锌粒,和氢离子反应,促进醋酸电离,所以醋酸根离子浓度增大,故正确;
故答案为:ABDE;
(6)加水稀释,酸性减弱,促进电离,n(CH3COO﹣)、n(H+)增大,但浓度减小,
A、氢离子浓度减小,故A错误;
B、加水稀释,促进电离,n(H+)增大,故B正确;
C、加水稀释,溶液接近中性,氢氧根离子浓度不再变化,故C错误;
D、醋酸的电离平衡常数不变,氢离子浓度减小,所以 ![]() 增大,故D正确;
增大,故D正确;
故答案为:BD.
(1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强;
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
(3)溶液越稀,越促进醋酸电离;
(4)溶液中氢离子浓度越小,对水的电离抑制程度越小;
(5)要使醋酸根离子浓度增大,可以采用加热、加入含有醋酸根离子的物质、加入和氢离子反应的物质;
(6)加水稀释,促进电离,n(CH3COO﹣)、n(H+)增大,但浓度减小,以此解答.

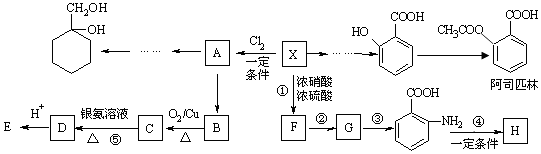
【题目】高锰酸钾可用于生活消毒,是中学化学常见的氧化剂。工业上,用软锰矿制高锰酸钾的流程如下:
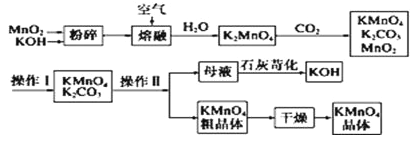
请回答下列问题:
(1)MnO2和KOH在熔融前粉碎的目的是_____________________________________________。
(2)写出二氧化锰和氢氧化钾熔融物中通入空气时发生的主要反应的化学方程式___________。
(3)通入CO2后,生成的KMnO4与MnO2的物质的量之比为___________。
(4)上述流程中可以循环使用的物质有___________、___________(填化学式)。
(5)已知:常温下,Ksp[Mn(OH)2]=2.4×10-13工业上,调节pH可以沉淀废水中Mn2+,当pH=10时,溶液中c(Mn2+)=___________mol/L。
(6)操作Ⅰ的名称是___________,操作Ⅱ根据下表KMnO4和K2CO3两物质在溶解性上的差异,采用___________、___________(填操作步骤)得到KMnO4粗晶体。
| 10 | 20 | 30 | 40 | 60 |
K2CO3 | 109.0 | 111.0 | 114.0 | 117.0 | 126.0 |
KMnO4 | 4.3 | 6.3 | 9.0 | 12.6 | 22.1 |