题目内容
【题目】某高校的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示,下列说法正确的是( )
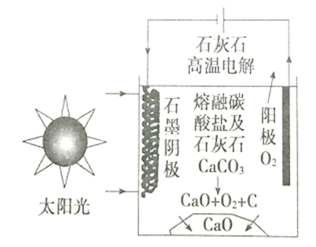
A. 该装置可以将太阳能转化为电能
B. 阴极的电极反应式为3CO2+4e—=C+2CO32—
C. 高温的目的只是为了将碳酸盐熔融,提供阴阳离子
D. 电解过程中电子由负极流向阴极,经过熔融盐到阳极,最后回到正极
【答案】B
【解析】
A. 由题图知,太阳能转化为化学能,该装置为电解池,将电能转化为化学能,故A错误;
B. 阴极发生还原反应,电极反应式为3CO2+4e—=C+2CO32—,故B正确;
C. 高温的目的是将碳酸盐熔融提供阴阳离子,将碳酸钙分解为氧化钙和二氧化碳,故C错误;
D. 电解过程中电子由负极流向阴极,阳极流向正极,熔融盐中没有电子移动,故D错误。
答案选B。

【题目】天然气是一种清洁的化石燃料,也是引起温室效应的一种物质。天然气的综合利用对节能减排、高效利用能源、减少二氧化碳排放有重大意义。作为化工原料,合成甲醇是天然气综合利用的重要途径。
CH4(g)+ CO2(g)![]() 2CO(g)+ 2H2(g)△H=+247.3 kJ·mol—1 ①
2CO(g)+ 2H2(g)△H=+247.3 kJ·mol—1 ①
CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H=+206.2 kJ·mol—1 ②
CO(g)+3H2(g) △H=+206.2 kJ·mol—1 ②
Ⅰ、合成甲醇的主要反应为:2H2(g)+ CO(g)![]() CH3OH(g) △H=-90.8 kJ·mol—1
CH3OH(g) △H=-90.8 kJ·mol—1
(1)该反应熵变△S________0(填“>、=或<”),该反应在______(填“高温”或“低温”)条件下能自发进行。
(2)生产过程中,合成气要循环,其目的是:________________________________。
(3)T℃下此反应的平衡常数为160。某时刻测得各组分的浓度如下,比较此时正、逆反应速率的大小:υ(正)________υ(逆)(填“>”“<”或“=”)
物质 | H2 | CO | CH3OH |
浓度/(mol·L—1) | 0.20 | 0.10 | 0.40 |
(4)在恒温恒容条件下,充入一定量的H2和CO,发生上述反应,则该反应达到平衡状态的标志有(__________________)
A.混合气体的密度保持不变 B.混合气体的总压强保持不变
C.甲醇的浓度保持不变 D.υ正(H2)= υ逆(CH3OH)
(5)在恒温恒容条件下,要提高反应2H2(g)+ CO(g)![]() CH3OH(g)中CO的转化率,可以采取的措施是(______________)
CH3OH(g)中CO的转化率,可以采取的措施是(______________)
A.升温 B.加入催化剂 C.增加CO的浓度
D.增加H2的浓度 E.充入惰性气体 F.分离出甲醇
Ⅱ、合成甲醇的另一反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-akJ·mol-1(a>0)。
CH3OH(g)+H2O(g) △H=-akJ·mol-1(a>0)。
在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生上述反应,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
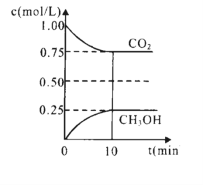
(6)下列措施中能使n(CH3OH )/n(CO2 )增大的是______(填编号)。
A.升高温度
B.恒温恒容下充入He(g)
C.将H2O(g)从体系中分离
D.恒温恒容再充入2 mol CO2和3 mol H2
(7)经计算该温度下此反应的平衡常数K=0.20 L2·mol—2。若改变条件_________(填选项),可使K=1。
A.增大压强 B.增大反应物浓度 C.降低温度
D.升高温度 E.加入催化剂
(8)10min内,用H2表示的该反应的化学反应速率为=_________mol·L—1·min—1



