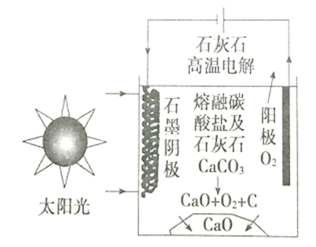
��Ŀ����
����Ŀ��(1)��һ�������£�ʹ26 g CO��O2�Ļ�������ַ�Ӧ�����û�����ڳ�������������Na2O2���巴Ӧ�������������14 g����ԭ���������CO��O2�������ȿ�����____________��
(2)ijͬѧ��һ��ʵ���з��֣���������ˮ��μӵ����з�̪��NaOH��Һ�У����ӵ����һ��ʱ��Һ�ĺ�ɫͻȻ��ʧ��
��ͬѧ������Һ�ĺ�ɫͻȻ��ʧ����ԭ�������̽����
�ٲ²⣺a.��ˮ�е������к���NaOH��ʹ��̪�ɺ�ɫ��Ϊ��ɫ��
b._____________��
�������һ��ʵ�鷽����֤�����²⣺____________
���𰸡�7��6�� 9��4 ��ˮ�еĴ�������Ư���ԣ�ʹ��̪��ɫ ���Ѿ���ɫ����Һ�еμ�NaOH��Һ������������ɫ���³��֣���²�a��ȷ������ɫ���ٳ���(��ɫ)����²�b��ȷ��
��������
(1)����2Na2O2+2CO2=2Na2CO3+O2����֪�����ȼ�պ��ڳ����¸�������Na2O2���巴Ӧ���ɹ���ΪNa2CO3��1 mol Na2O2����1 mol Na2CO3��������������28 g��ǡ��Ϊ��ΪCO2��CO���������Դ��ж�ԭ����������������֮�ȣ�
(2)��̪�ڼ��Ի������Ժ�ɫ��������ˮ��Ӧ��������ʹ����ᣬ����ʹ����ᶼ�������ԣ������кͷ�Ӧ��ʹ��Һ���Լ�������Һ�ĺ�ɫ��dz������ʧ�����Ҵ��������ھ���ǿ�����ԣ���ʹ���ʷ��ӽṹ�����ı䣬��Һ�ɺ�ɫ��Ϊ��ɫ����ɫԭ���ͨ������ɫ�����Һ���ٵμ����������������������Ƿ��ٻָ���ɫ�жϣ��ݴ˽��
(1) CO��O2��һ�������·�����Ӧ��2CO+O2![]() 2CO2��������CO2��Na2O2������2Na2O2+2CO2=2Na2CO3+O2�����ݷ���ʽ��֪��ȼ�ղ�����CO2�ڳ�������������Na2O2���巴Ӧ���ɹ���ΪNa2CO3��1 mol Na2O2����1 mol Na2CO3��������������28 g��ǡ��Ϊ��ΪCO2��CO����������������14 g��˵��������Ӧ��2CO+O2
2CO2��������CO2��Na2O2������2Na2O2+2CO2=2Na2CO3+O2�����ݷ���ʽ��֪��ȼ�ղ�����CO2�ڳ�������������Na2O2���巴Ӧ���ɹ���ΪNa2CO3��1 mol Na2O2����1 mol Na2CO3��������������28 g��ǡ��Ϊ��ΪCO2��CO����������������14 g��˵��������Ӧ��2CO+O2![]() 2CO2��COΪ14 g�������ʵ�����0.5 mol���䷴Ӧ���ĵ�O2�����ʵ���Ϊ0.25 mol����ӦO2����Ϊm(O2)=0.25 mol��32 g/mol=8 g��14 g+8 g=22 g<26 g���������4 g��˵��CO��O2����ǡ�÷�Ӧ����һ�����������������������ΪO2����m(CO)=14 g��m(O2)=8 g+4 g=12 g��m(CO)��m(O2)=14��12=7��6��������������ΪCO����m(CO)=14 g+4 g=18 g��m(O2)=8 g��m(CO)��m(O2)=18��8=9��4��
2CO2��COΪ14 g�������ʵ�����0.5 mol���䷴Ӧ���ĵ�O2�����ʵ���Ϊ0.25 mol����ӦO2����Ϊm(O2)=0.25 mol��32 g/mol=8 g��14 g+8 g=22 g<26 g���������4 g��˵��CO��O2����ǡ�÷�Ӧ����һ�����������������������ΪO2����m(CO)=14 g��m(O2)=8 g+4 g=12 g��m(CO)��m(O2)=14��12=7��6��������������ΪCO����m(CO)=14 g+4 g=18 g��m(O2)=8 g��m(CO)��m(O2)=18��8=9��4��
(2)��������ˮ������Ӧ��Cl2+H2O=HCl+HClO�����з�̪��NaOH��Һ��ɫ���ܵ�ԭ��һ��������ˮ�е�ǿ���������������Ʒ����кͷ�Ӧ��������NaOH��ʹ��Һ�ļ��Լ������������еĴ��������ǿ�����ԣ�����Ư���ԣ�ʹ��ɫ�����ʷ���������Ϊ��ɫ���ʷ��ӣ��Ӷ�ʹ��Һ��ɫ��ȥ��
��Ҫ֤����ɫ��ȥ��ԭ��������кͻ�������Ư�ף������Ѿ���ɫ����Һ�м�������NaOH��Һ��������ʹ��Һ�ʼ��ԣ�����ʱ��Һ�ָ���ɫ��˵���Ǽ���к͵��£������������Һ��Ϊ��ɫ����˵����ɫ�DZ����ڴ���������Ư��Ե�ʡ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ����ͼ��Ԫ�����ڱ���һ���֣���Ҫ��ش����⣺
�� | �� | ||||||||||||||||
�� | �� | �� | �� | �� | �� | �� | �� | ||||||||||
�� | �ޡ� | �� | �� | �� | �� | �� | �� | �� | �� | �� | �� | �� | �� | �� | �ࡡ | �� | �� |
(1)Ԫ�آ������ڱ���λ����_______��Ԫ�آ۵����������Ļ�ѧʽΪ________��
(2)Ԫ�آ٢���ɻ��������ʽΪ___________��
(3)Ԫ�آڵĵ�����������������ˮ�����ȵ�Ũ��Һ��Ӧ�Ļ�ѧ����ʽΪ___��
(4)Ԫ�آ�����γɵĻ�������Ԫ�آ۵��⻯���ˮ��Һ��Ӧ�����ӷ���ʽΪ_____��
(5)Ԫ�آܢݢޢ��γɵļ����ӣ������Ӱ뾶��С�����˳��Ϊ_____(�����ӷ��ű�ʾ)��
(6)A��F������ͼ��ʾ��ת����A��B��C��DΪ��������ij��Ԫ���γɵĵ��ʣ�E��F��GΪB��C��D��A�γɵĶ�Ԫ�����G��һ�ֳ����������壬��B���Է�Ӧ����E��E��BԪ�ص���������Ϊ60%��FΪ�������ʡ�
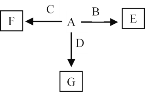
��A��F�Ļ�ѧʽ�ֱ�Ϊ_______��_______��
��B��G��Ӧ�Ļ�ѧ����ʽΪ____________________��
��C��NaOH��Һ��Ӧ�����ӷ���ʽΪ______________��