题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A、常温下,
| ||
| B、加入Mg能放出H2的溶液:Na+、Al3+、Cl-、SO42- | ||
| C、加入苯酚显紫色的溶液:NH4+、K+、Cl-、S2- | ||
| D、由水电离产生的c(H+)=1×10-12的溶液:NH4+、Na+、AlO2-、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.常温下,
=1010的溶液,c(H+)=0.01mol/L,呈酸性;
B.加入Mg能放出H2的溶液呈酸性;
C.加入苯酚显紫色的溶液含有Fe3+;
D.由水电离产生的c(H+)=1×10-12的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性.
| c(H+) |
| c(OH-) |
B.加入Mg能放出H2的溶液呈酸性;
C.加入苯酚显紫色的溶液含有Fe3+;
D.由水电离产生的c(H+)=1×10-12的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性.
解答:
解:A.常温下,
=1010的溶液,c(H+)=0.01mol/L,呈酸性,Fe2+与NO3-发生氧化还原反应而不能大量共存,故A错误;
B.加入Mg能放出H2的溶液呈酸性,离子之间不发生任何反应,可大量共存,故B正确;
C.加入苯酚显紫色的溶液含有Fe3+,与S2-反应而不能大量共存,故C错误;
D.由水电离产生的c(H+)=1×10-12的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,酸性条件下AlO2-、HCO3-不能大量共存,碱性条件下NH4+、HCO3-不能大量共存,且AlO2-与NH4+、HCO3-反应而不能大量共存,故D错误.
故选B.
| c(H+) |
| c(OH-) |
B.加入Mg能放出H2的溶液呈酸性,离子之间不发生任何反应,可大量共存,故B正确;
C.加入苯酚显紫色的溶液含有Fe3+,与S2-反应而不能大量共存,故C错误;
D.由水电离产生的c(H+)=1×10-12的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,酸性条件下AlO2-、HCO3-不能大量共存,碱性条件下NH4+、HCO3-不能大量共存,且AlO2-与NH4+、HCO3-反应而不能大量共存,故D错误.
故选B.
点评:本题考查离子共存问题,为高考常见题型和高频考点,侧重于学生的分析能力以及元素化合物知识的综合理解和运用的考查,注意把握题目要求以及常见离子的性质和反应类型的判断,答题时注意题给信息,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列根据反应原理设计的实际应用不正确的是( )
| A、CO32-+H2O?HCO3-+OH-;用热的纯碱溶液清洗油污 |
| B、SnCl2+H2O?Sn(OH)Cl+HCl;配制氯化亚锡溶液时加入氢氧化钠溶液 |
| C、A13++3HCO3-═Al(OH)3↓+3CO2↑;泡沫灭火器灭火 |
| D、A13++3H2O?Al(OH)3(胶体)+3H+;明矾净水 |
化学与生产、生活、社会密切相关,下列说法正确的是( )
| A、漂白粉、漂粉精可用来漂白棉、麻、纸张,不能用作游泳池及环境的消毒剂 |
| B、硫酸工业中,从吸收塔上部导出的气体再次通入接触室进行二次氧化,进一步吸收后,二氧化硫的含量很少,可直接排放到空气中 |
| C、工业上可用氯化钠制备化肥NH4Cl |
| D、PM2.5是指大气中直径小于或等于2.5微米的颗粒物,PM2.5比胶体粒子小,因其比表面积大,故可吸附重金属离子,入肺后对人体产生很大的危害 |
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A、1mol甲基含有电子数为9NA | ||
| B、常温下,1mol乙烯和乙硼烷(B2H6)的混合气体,所含的电子数为16NA | ||
C、标准状况下,1L庚烷所含有的分子数约为
| ||
| D、26g乙炔和苯蒸气的混合气体中所含的碳原子数为2NA |
2.8g Fe全部溶于一定浓度200mL的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液中c(H+ )=0.1mol?L-1.若反应前后溶液体积变化忽略不计,则下列有关判断正确的是( )
| A、反应后溶液中存在Fe3+和Fe2+ |
| B、1.12L气体是NO、NO2的混合气体 |
| C、反应后溶液中c(NO3-)=0.85mol?L-1 |
| D、反应后的溶液最多还能溶解1.4g Fe |
下列判断正确的是( )
| A、同温下,HF比HClO易电离,则NaF溶液的pH比NaClO溶液的pH大 |
| B、常温下,0.4mol?L-1 HA溶液和0.2mol?L-1 NaOH溶液等体积混合后的pH等于3,则混合溶液中粒子浓度大小关系:c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-) |
| C、常温下,BaSO4在饱和Na2SO4溶液中的Ksp比在纯水中的Ksp小 |
| D、用铂电极电解食盐水,一段时间后两极产生气体体积比为3:2(同条件下),为将电解液恢复原状,则只需向电解液中通入一定量的HCl气体 |
在25℃的条件下,下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42-)=c(NH4+) |
| B、pH=3的醋酸溶液,稀释至原体积的10倍后pH=4 |
| C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液pH<7 |
| D、向0.1mol?L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)增大 |
各取1mol下列物质(除苯环外,分子内不含其他类环)与浓溴水充分反应,消耗Br2的物质的量按①②顺序排列正确的是( )
①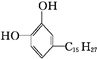 ②
②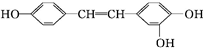
①
 ②
②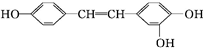
| A、2mol、6mol |
| B、5mol、6mol |
| C、4mol、5mol |
| D、3mol、6mol |