题目内容
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A、1mol甲基含有电子数为9NA | ||
| B、常温下,1mol乙烯和乙硼烷(B2H6)的混合气体,所含的电子数为16NA | ||
C、标准状况下,1L庚烷所含有的分子数约为
| ||
| D、26g乙炔和苯蒸气的混合气体中所含的碳原子数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据甲基是取代基,结合结构计算电子数;
B、依据乙烯和乙硼烷(B2H6)分子中所含的电子数计算分析判断;
C、标准状况庚烷不是气体;
D、乙炔和苯的实验式相同,计算26gCH中碳原子数;
B、依据乙烯和乙硼烷(B2H6)分子中所含的电子数计算分析判断;
C、标准状况庚烷不是气体;
D、乙炔和苯的实验式相同,计算26gCH中碳原子数;
解答:
解:A、甲基是取代基,1mol甲基含有电子数为9NA,故A正确;
B、乙烯和乙硼烷分子中都含16个电子,常温下,1mol乙烯和乙硼烷(B2H6)的混合气体,所含的电子数为16NA,故B正确;
C、庚烷标况下为非气体,故C错误;
D、乙炔和苯的实验式相同,计算26gCH中碳原子数为2NA,故D正确;
故选C.
B、乙烯和乙硼烷分子中都含16个电子,常温下,1mol乙烯和乙硼烷(B2H6)的混合气体,所含的电子数为16NA,故B正确;
C、庚烷标况下为非气体,故C错误;
D、乙炔和苯的实验式相同,计算26gCH中碳原子数为2NA,故D正确;
故选C.
点评:本题考查了阿伏伽德罗常数的分析,主要是物质结构的分析判断,气体摩尔体积条件应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
反应3H2(g)+N2(g)?2NH3(g)△H=-46.19kJ?mol-1,关于这个反应的平衡常数K,下列说法正确的是( )
| A、随温度升高K增加 |
| B、随压强升高K增加 |
| C、随温度升高K减小 |
| D、随压强升高K减小 |
下列反应中,生成的有机物只有一种的是( )
A、异戊二烯(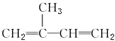 )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 |
| B、2氯丁烷与NaOH乙醇溶液共热发生消去HCl分子的反应 |
| C、新戊烷和氯气发生取代反应生成一氯取代物 |
| D、甲苯在一定条件下发生硝化反应生成一硝基甲苯 |
下列说法不正确的是( )
| A、长期使用阿司匹林会出现水杨酸中毒表现,应立即停药,静脉注射碳酸氢钠溶液 |
| B、红宝石、水晶、钻石的主要成分都是硅酸盐 |
| C、高温条件下可杀死H7N9型禽流感病毒,属于蛋白质的变性 |
| D、石油裂解、煤的气化、海水制镁都包含化学变化 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A、常温下,
| ||
| B、加入Mg能放出H2的溶液:Na+、Al3+、Cl-、SO42- | ||
| C、加入苯酚显紫色的溶液:NH4+、K+、Cl-、S2- | ||
| D、由水电离产生的c(H+)=1×10-12的溶液:NH4+、Na+、AlO2-、HCO3- |
分别将下列物质:①FeCl3②Na2O2③NaCl④Ca(HCO3)2投入水中,对其溶液加热蒸干,仍能得到原物质的是( )
| A、①②③ | B、①③ | C、③④ | D、③ |
下列离子方程式正确的是( )
| A、向FeCl3溶液中加入Fe粉:2Fe3++Fe═3Fe2+ |
| B、向AlCl3溶液中滴加氨水:Al3++4OH-═AlO2-+2H2O |
| C、NaOH溶液中通入少量二氧化硫:SO2+2OH-═SO32-+H2O |
| D、用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ |
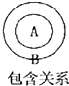
在物质分类中常存在包含关系如图B包含A,下列关系中前者包含后者.其中错误的是( )

| A、有机物 烃 |
| B、烃 脂肪烃 |
| C、脂肪烃 烯烃 |
| D、烯烃 氯乙烯 |