题目内容
12.15号元素在周期表中的位置第3周期第VA族,其最高正化合价为+5.分析 周期序数=电子层数,主族元素最外层电子数等于族序数,也等于最高正化合价,由此分析解答.
解答 解:15号元素三个电子层,最外层5个电子,所以位置为第3周期第VA族,最高正化合价为+5,故答案为:第3周期第VA族;+5.
点评 本题考查了元素在周期表中位置的判断,明确元素原子核外电子层数与周期数、最外层电子数与主族族序数之间的关系是解本题关键,根据其原子结构示意图来确定元素的位置即可,原子核外电子排布规律为学习难点,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列说法正确的是( )
| A. | 2015年2月15日起,湖南省环保厅按照《环境空气质量标准》(GB3095-2012)发布了全省14市州政府所在地城市空气质量排名,主要污染物包括PM2.5、PM10、O3、CO2、SO2和NO2等6项指标 | |
| B. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 | |
| C. | 明矾水解产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒 | |
| D. | 将实验室的废酸液和废碱液中和后再排放符合“绿色化学”的要求 |
20.下列过程中,离子键被破坏的是( )
| A. | 溴挥发 | B. | 氯气被木炭吸附 | C. | 硫酸溶于水 | D. | 食盐溶于水 |
17.某元素最高价氧化物对应水化物的化学式为H2XO3,这种元素的气态氢化物的化学式是( )
| A. | HX | B. | XH4 | C. | XH3 | D. | H2X |
4.下列叙述中正确的是( )
| A. | 周期表中第VA族元素的最高价氧化物对应水化物的化学式均为H3RO4 | |
| B. | O${\;}_{2}^{2-}$与S2-具有相同的质子数和电子数 | |
| C. | 氕、氘、氚分别与O原子形成的水H2O、D2O、T2O的化性质不同 | |
| D. | 形成离子键的阴阳离子间只存在静电吸引力 |
1.如图所示烧杯中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )


| A. | (3)(4)(2)(1) | B. | (3)(1)(4)(2) | C. | (4)(3)(1)(2) | D. | (3)(4)(1)(2) |
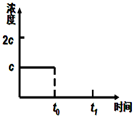 请你利用所学反应原理知识解决下列问题:
请你利用所学反应原理知识解决下列问题:
 ;A→F
;A→F .
.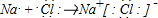 .
. .
. ②NaOH
②NaOH ③NH3
③NH3 ④N2
④N2
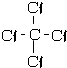 ③NH3
③NH3 ④H2SH-S-H.
④H2SH-S-H.