题目内容
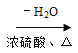
【题目】(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式 _。
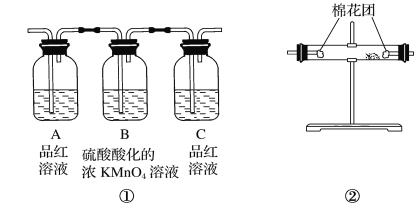
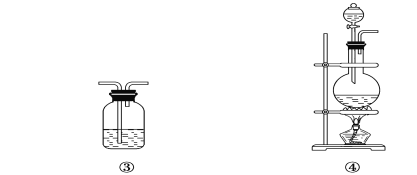
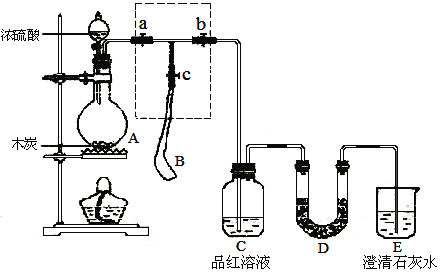
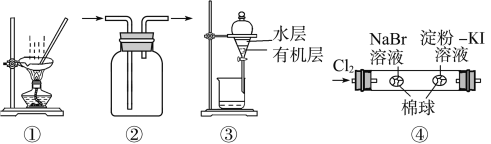
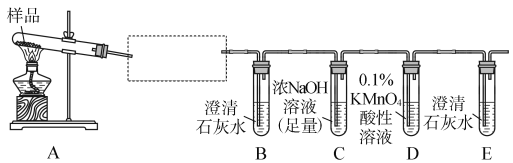
(2)试用上图所示各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气体从左至右的流向)是________→________→________→________(填装置的编号)。
(3)怎样检查整套装置的气密性
(4)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色,A瓶溶液的作用是________,B瓶溶液的作用是________,C瓶溶液的作用是________。
(5)装置②中所加的固体药品是________,可验证的产物是________。
(6)装置③中所盛溶液是________,可验证的产物是________。
【答案】(1)C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O(2分)
CO2↑+2SO2↑+2H2O(2分)
(2)④ ② ① ③(2分)
(3)关闭分液漏斗活塞,微热烧瓶,③导管口产生气泡,停止加热后③导管中有一段稳定的液柱,则气密性良好(2分)
(4)验证SO2的存在(1分) 充分吸收SO2(1分) 验证SO2是否已被吸收完全(1分)
(5)无水硫酸铜(1分) 水(1分)(6)澄清的石灰水(1分) CO2(1分)
【解析】
试题分析:(1)碳可以和浓硫酸反应生成二氧化碳、二氧化硫以及水,反应的方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;
CO2↑+2SO2↑+2H2O;
(2)检验二氧化碳和二氧化硫时用到的溶液中均含有水,所以先检验水的存在,二氧化碳和二氧化硫均可以使澄清石灰水变浑浊,所以先检验二氧化硫,再除去,最后检验二氧化碳,连接顺序④→②→①→③;
(3)根据装置结构可知检验气密性的实验操作是:关闭分液漏斗活塞,微热烧瓶,③导管口产生气泡,停止加热后③导管中有一段稳定的液柱,则气密性良好。
(4)根据检验的顺序,在检验二氧化碳之前先检验二氧化硫,可以用品红来检验,除二氧化硫可以用高锰酸钾,二氧化硫是否被高锰酸钾吸收干净,也可以用品红来检验,所以A瓶溶液的作用是验证SO2的存在,B瓶溶液的作用是充分吸收SO2,C瓶溶液的作用是验证SO2是否已被吸收完全;
(5)根据以上分析可知用无水硫酸铜来检验水的产生,则装置②中所加的固体药品是无水硫酸铜。
(6)根据以上分析可知可以用澄清石灰水检验二氧化碳的存在,因此装置③中所盛溶液是澄清的石灰水。

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案【题目】I.某次采集酸雨样品,每隔一段时间测定一次pH,得到数据如下:
时间 | 开始 | 8小时 | 16小时 | 24小时 | 32小时 | 40小时 | 48小时 |
pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(1)放置时,雨水样品酸性_______________(填“增强”、“减弱”或“不变”)。
酸性变化的原因_________________________________(用化学方程式表示)。
II.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(2) 写出一氧化碳与一氧化氮反应的化学方程式:__________________________。
(3) 在“催化转化器”转化后的气体中有CO2、SO2,下列不能鉴别这两种气体的是(____)
A.KMnO4溶液 B.石灰水 C.BaCl2溶液 D.品红溶液
(4) 有效减少城市污染的方法可以有____________
A. 开发氢能源 B. 使用电动车 C. 植树造林 D. 戴上呼吸面具