题目内容
1.按要求完成下列问题(1)甲基的电子式

(2)通式为CnH2n+2的最简单同系物的分子式CH4
(3)相对分子质量为72且沸点最低的烷烃的结构简式CH3C(CH3)2CH3.
分析 (1)甲基中碳原子有1个单电子;
(2)最简单的烷烃为甲烷;
(3)设烷烃的分子式为CxH(2x+2),根据相对分子质量为72,列出方程式进行计算x值,支链越多,沸点越低.
解答 解:(1)甲基中碳原子有1个单电子,甲基电子式为 ,故答案为:
,故答案为: ;
;
(2)通式为CnH2n+2的为烷烃的通式,最简单的烷烃为甲烷,分子式为:CH4,故答案为:CH4;
(3)设烷烃的分子式为CxH(2x+2),则14x+2=72,解得x=5,所以该烷烃的分子式为C5H12,
分子式为C5H12的同分异构体有主链有5个碳原子的:CH3CH2CH2CH2CH3,
主链有4个碳原子的:CH3CH(CH3)CH2CH3,
主链有3个碳原子的:CH3C(CH3)2CH3;
支链越多,沸点越低,故CH3C(CH3)2CH3,故答案为:CH3C(CH3)2CH3.
点评 本题主要考查了电子式书写、烷烃的通式、命名方法的应用、有机物结构简式的书写,难度不大,注意主链选择,位置编号的正确选择.

练习册系列答案
相关题目
18.在可逆反应CO(g)+H2O(g)?CO2(g)+H2(g)(正反应为放热反应)中,改变下列条件,不能使v正增大的是( )
| A. | 升高温度 | B. | 降低温度 | C. | 使用催化剂 | D. | 增大CO浓度 |
9.已知热化学方程式2SO2(g)+O2(g)?2SO3(g)△H=-QkJ/mol(Q>0),则下列说法正确的是( )
| A. | 2molSO2(g)和1molO2(g)所具有的内能小于2molSO3(g)所具有的内能 | |
| B. | 将2molSO2(g)、1molO2(g)置于一密闭容器中充分反应后放出QkJ的热量 | |
| C. | 升高温度,平衡向逆反应移动,上述热化学方程式中的Q值减小 | |
| D. | 如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热QkJ,则此过程中有2molSO2(g)被氧化 |
16.按反应特征与产物的结构关系,有机反应大致可分为:取代反应、消去反应、加成反应三种,下列变化中不属于取代反应的是( )
| A. | C6H5CH2Cl+NaCN-→C6H5CH2CN+NaCl | B. | 2Na+2 C2H5OH-→2C2H5ONa+H2↑ | ||
| C. | CH3CH2CHO+HCN-→CH3CH2CH(CN)OH | D. | CH3COOC2H5+H2O-→CH3COOH+C2H5OH |
6.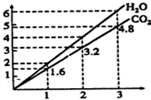 两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )
①一定有C2H4 ②一定有CH4③一定有C3H8④一定没有C2H6 ⑤可能有C2H2.
 两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )①一定有C2H4 ②一定有CH4③一定有C3H8④一定没有C2H6 ⑤可能有C2H2.
| A. | ②⑤ | B. | ②④ | C. | ③④ | D. | ①③ |
13.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小 | |
| C. | 放热反应在常温下一定很容易发生 | |
| D. | 化学反应一定有新物质的生成,但不一定有能量的变化 |
10.下列有关元素的性质及其递变规律正确的是( )
| A. | 第二周期元素从左到右,最高正价从+1递增到+7 | |
| B. | ⅠA和ⅦA族元素间可形成离子化合物和共价化合物 | |
| C. | 同主族元素的简单阴离子还原性越强,元素非金属性越强 | |
| D. | 同周期金属元素的化合价越高,其金属性越强 |
 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答: