题目内容
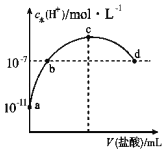
【题目】下列实验结果与图像相符的是( )
A.向含有盐酸、氯化镁和氯化铝的溶液中逐滴加入NaOH溶液直至过量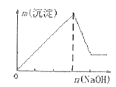
B.向澄清石灰水中通入CO2气体直至过量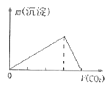
C.向NaAlO2溶液中逐滴加入盐酸直至过量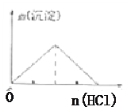
D.向AlCl3溶液中逐滴加入氨水直至过量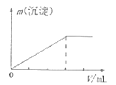
【答案】D
【解析】
A.将氢氧化钠溶液滴入某混有盐酸的氯化镁和氯化铝的混合溶液中,盐酸优先与NaOH溶液反应,所以开始时不会生成沉淀。当盐酸完全反应后,镁离子、铝离子与氢氧化钠反应生成氢氧化镁、氢氧化铝沉淀。当镁离子、铝离子完全反应后,氢氧化铝与过量的氢氧化钠溶液反应,导致沉淀部分溶解,图象中沉淀的量减少,图象变化开始不符合反应过程,A错误;
B.石灰水中通入二氧化碳,先发生![]() ,生成沉淀,后发生
,生成沉淀,后发生![]() ,故先产生沉淀,后沉淀溶解,前后两部分二氧化碳的物质的量为1:1,图象不符合,B错误;
,故先产生沉淀,后沉淀溶解,前后两部分二氧化碳的物质的量为1:1,图象不符合,B错误;
C.向![]() 溶液中逐滴加入盐酸,先产生氢氧化铝沉淀,继续滴加盐酸,
溶液中逐滴加入盐酸,先产生氢氧化铝沉淀,继续滴加盐酸,![]() 和HCl溶液反应,生成氯化铝和水,沉淀溶解,生成沉淀和沉淀溶解消耗HCl的比为1:3,图象不符合;C错误;
和HCl溶液反应,生成氯化铝和水,沉淀溶解,生成沉淀和沉淀溶解消耗HCl的比为1:3,图象不符合;C错误;
D.向![]() 溶液中加入氨水,反应生成氢氧化铝沉淀,再加氨水,沉淀不能溶解,只发生的离子反应为Al3++3NH3H2O=Al(OH)3↓+3NH4+,图象符合,D正确。
溶液中加入氨水,反应生成氢氧化铝沉淀,再加氨水,沉淀不能溶解,只发生的离子反应为Al3++3NH3H2O=Al(OH)3↓+3NH4+,图象符合,D正确。
答案选D。

 名校课堂系列答案
名校课堂系列答案【题目】工业上从电解精炼铜的阳极泥(成分为CuS、Cu2Se、Cu2Te 和少量金属单质Au) 中回收碲、硒的工艺流程如下:

已知:①TeO2是两性氧化物。
②Se和TeO2的物理性质如下:
物理性质 | 熔点 | 沸点 | 水溶性 |
Se | 221℃ | 685℃ | 难溶于水 |
TeO2 | 733℃ | 1260℃ | 微溶于水 |
(1)Se在周期表中的位置为____________。
(2)SeO2与SO2的混合烟气可用水吸收制得单质Se,当有2 mol电子转移时,会生成______mol Se。过滤所得粗硒可采用真空蒸馏的方法提纯获得纯硒,采用真空蒸馏的目的是_______________。
(3)“碱浸”过滤得到滤渣的主要成分是_______(填化学式)。
(4)“沉碲”时控制溶液的pH为4.5-5.0,生成TeO2沉淀。如果H2SO4的浓度过大,将导致“沉碲”不完全,原因为_______________________________________。
(5)“酸溶”将TeO2先溶于硫酸得到Te(SO4)2,然后加入Na2SO3溶液进行还原,还原碲的离子反应方程式是_______________________________________。
(6)常温下,SeO2与NaOH溶液反应所得NaHSeO3溶液的pH______7(填“>”“<”或“=”),请通过计算说明_____________________________。(已知25℃时,亚硒酸(H2SeO3)的Ka1=2.5×10-3,Ka2=2.5×10-7)
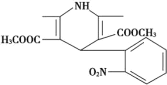
【题目】碳酸二乙酯(![]() )常温下为无色清澈液体。主要用作硝酸纤维素、树脂和一些药物的溶剂,或有机合成的中间体。现用下列装置制备碳酸二乙酯。
)常温下为无色清澈液体。主要用作硝酸纤维素、树脂和一些药物的溶剂,或有机合成的中间体。现用下列装置制备碳酸二乙酯。
化学式 | 熔点/℃ | 沸点/℃ | 物理性质 |
COCl2 | -118 | 8.2 | 微溶于水,溶于芳烃、苯、四氯化碳、氯仿、乙酸等多数有机溶剂,遇水迅速水解,生成氯化氢 |
SO3 | 16.8 | 44.8 | 溶于水,并与水反应生成硫酸和放出大量的热 |
SO2Cl2 | -54.1 | 69.1 | 溶于乙酸、苯,与水反应生成H2SO4和HCl |
CCl4 | -22.9 | 76.8 | 微溶于水,易溶于多数有机溶剂 |
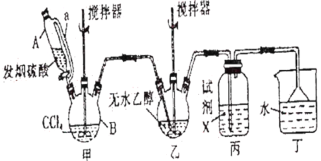
回答下列问题:
(1)甲装置主要用于制备光气(COCl2),先将仪器B中的四氯化碳加热至55~60℃,再缓缓滴加发烟硫酸。
①仪器B的名称是__________。
②仪器A的侧导管a的作用是__________。
(2)试剂X是__________,其作用是__________。
(3)丁装置除了吸收COCl2外,还能吸收的气体是__________(填化学式)。仪器B中四氯化碳与发烟硫酸(用SO3表示)反应只生成两种物质的量为1:1的产物,且均易与水反应,写出该反应化学方程式:__________。
(4)无水乙醇与光气反应生成氯甲酸乙酯,再继续与乙醇反应生成碳酸二乙酯。
①写出无水乙醇与光气反应生成氯甲酸乙酯的化学方程式:__________。
②若起始投入92.0g无水乙醇,最终得到碳酸二乙酯94.4g,则碳酸二乙酯的产率是__________(三位有效数字)