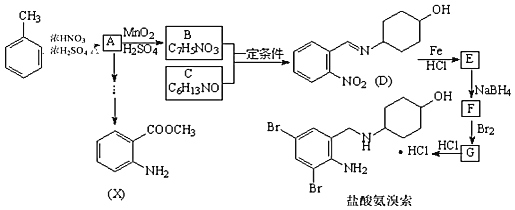
题目内容
【题目】一种新药物结构如图所示,下列有关该化合物说法正确的是
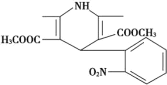
A.分子式为C17H17N2O6
B.能发生水解反应、聚合反应、取代反应、消去反应
C.分子中含有四种不同的官能团
D.能与氢气发生加成反应,但不能与溴的四氯化碳溶液反应
【答案】C
【解析】
由该有机物的结构简式可知分子式,其分子中含-COOC-、碳碳双键、氨基、硝基,结合酯、烯烃等有机物的性质来解答。
A.根据该有机物的结构简式可知,其分子式为C17H18N2O6,故A错误;
B.该有机物含-COOC-可发生水解、取代反应,含碳碳双键可发生聚合反应,不能发生消去反应,故B错误;
C.该有机物含-COOC-、碳碳双键、氨基、硝基四种官能团,故C正确;
D.该有机物含碳碳双键,故其可与氢气发生加成反应,也能与溴的四氯化碳溶液发生加成反应,故D错误;
故答案为C。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】(1)请用下列10种物质的序号填空:①O2②H2③NH4NO3④K2O2⑤Ba(OH)2⑥CH4⑦CO2⑧NaF ⑨NH3⑩I2
既有离子键又有非极性键的是________;既有离子键又有极性键的是________。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为:______________;若XY2为共价化合物时,其结构式为:__________________。
(3)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190℃(2.02×103Pa),但在180℃就开始升华,据此判断,氯化铝是________(填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据是____________________。
(4)现有a~g 7种短周期元素,它们在周期表中的位置如下,请据此回答下列问题:
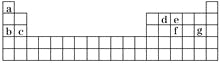
①元素的原子间反应最容易形成离子键的是________(填序号,下同),容易形成共价键的是______;
A.c和f | B.b和g | C.d和g | D.b和e |
②写出a~g 7种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式______。
【题目】下表中列出了25C、101kPa时一些物质的燃烧热数据
物质 | CH4 | C2H2 | H2 |
燃烧热/( kJ·mol-1) | 890.3 | 1299.6 | 285.8 |
已知键能:C—H键:413.4 kJ·mol-1、H—H键:436 kJ·mol-1,乙炔的结构是为H—C![]() C—H则下列叙述正确的是( )
C—H则下列叙述正确的是( )
A.2H2(g) + 2O2(g) = 2H2O(g) ΔH = -571.6 kJ·mol-1
B.CH4和C2H2中所含化学键完全相同
C.2CH4(g) = C2H2(g) + 3H2(g) ΔH = -376.4 kJ·mol-1
D.C![]() C键能为796 kJ·mol-1
C键能为796 kJ·mol-1