题目内容
2.利用图1所示实验(部分装置)收集氯气并验证氯气的性质: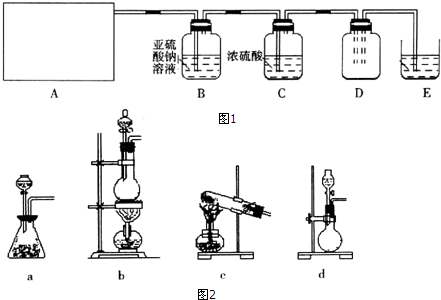
(1)A为Cl2的发生装置.若制取氯气的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,与之对应的A装置(图2)是b(填写装置的序号).
(2)利用D中的广口瓶收集氯气,试在装置图中完善D装置(将虚线表示的一根或两根导管改为实线,也可都不改).
(3)写出装置E中反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
(4)利用D中收集的氯气进行铁与氯气的反应实验:用坩埚钳夹持一束细铁丝,在酒精烧至红热,然后伸入盛有氯气的集气瓶中.
(5)通入氯气一段时间后,洗气瓶B溶液中有一部分SO32-氧化成SO42-,反应的离子方程式为SO32-+Cl2+H2O=SO42-+2Cl-+2H+.试设计实验方案,检验洗气瓶B溶液中Cl和SO42-的存在.可供选择的试剂及仪器为:
稀盐酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液、AgNO3溶液、澄清石灰水、试管、胶头滴管.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量B中溶液于试管Ⅰ中,滴加过量稀盐酸和BaCl2溶液 | 若产生白色沉淀,则洗气瓶B溶液中存在SO42- |
| 步骤2:另取适量B中溶液于试管Ⅱ中,滴加过量Ba(NO3)2溶液,振荡,静置 | 产生白色沉淀 |
| 步骤3:取步骤2后试管Ⅱ中的上层清液于试管Ⅲ中,滴加稀HNO3和AgNO3溶液. | 若产生白色沉淀,则洗气瓶白溶液中存在Cl- |
分析 (1)实验室通常用二氧化锰与浓盐酸加热反应制备氯气,依据反应物状态和反应条件选择发生装置;
(2)氯气的密度大于空气的密度,应选择向上排空气法;
(3)氢氧化钠与氯气反应生成氯化钠、次氯酸钠和水;
(4)依据氯气与铜反应的条件解答;
(5)氯气具有强的氧化性,能够氧化亚硫酸根离子生成硫酸根离子,据此写出反应离子方程式;
检验硫酸根离子应排除亚硫酸根离子的干扰;检验氯离子选用硝酸银,反应生成氯化银不溶于稀硝酸.
解答 解:(1)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水,方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,反应为固体+固体加热反应,应选择装置b;
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O; b;
(2)氯气的密度大于空气的密度,应选择向上排空气法,利用D中的广口瓶收集氯气,气体应长进短出,左边改为实线,
故答案为:左边改为实线;
(3)氢氧化钠与氯气反应生成氯化钠、次氯酸钠和水,反应离子方程式:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(4)氯气与铜反应需要加热,所以应将铜丝在酒精烧至红热,
故答案为:在酒精烧至红热;
(5)亚硫酸根离子具有强的还原性能够被氯气氧化生成硫酸根离子,反应的离子方程式为:Cl2+SO32-+H2O═SO42-+2H++2Cl-;
检验洗气瓶B溶液中SO42-的存在,应排除亚硫酸根离子,先加入足量的稀盐酸,然后加入氯化钡溶液,若出现白色沉淀,即含有硫酸根离子;
检验氯离子存在,应排除硫酸根、亚硫酸根离子的干扰,取适量洗气瓶B中溶液于试管Ⅱ中,滴加 过量Ba(NO3)2溶液振荡,静置,取上层清液于试管Ⅲ中,滴加硝酸银和稀硝酸,若产生白色沉淀,则洗气瓶B溶液中存在Cl-;
故答案为:Cl2+SO32-+H2O═SO42-+2H++2Cl-;过量稀盐酸和BaCl2溶液;稀HNO3和AgNO3溶液.
点评 本题为实验题,考查了氯气的制备、氯气性质的检验,明确反应的原理,发生装置选择的依据是解题关键,注意硫酸根、氯离子的检验方法,题目难度中等.

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案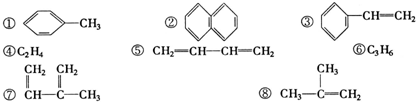
| A. | ①和 ② | B. | ④和⑥ | C. | ⑤和⑧ | D. | ④和⑧ |
| 元素代号 | X | Y | Z | Q | R | T |
| 原子半径/10-10m | 0.77 | 0.66 | 0.70 | 1.17 | 0.99 | 1.10 |
| 主要化合价 | +4、-4 | -2 | +5、-3 | +4、-4 | +7、-1 | +5、-3 |
| A. | X与Y可以形成阴离子XY32- | |
| B. | 元素R的氧化物对应水化物一定为强酸 | |
| C. | Z的氢化物的沸点比T的氢化物的沸点高 | |
| D. | 由X形成的化合物QX和XR4,其晶体类型不相同 |
| A. | 碳酸氢钠与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 大理石放入稀硝酸中:CO32-+2H+═CO2↑+H2O | |
| C. | 铝片插入浓烧碱溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 稀硫酸与氢氧化钡溶液混合:Ba2++SO42-═BaSO4↓ |
| A. | 工业上常采用电解法冶炼Y 单质 | |
| B. | 气态氢化物的稳定性:H2W强于H2Z | |
| C. | 离子半径由大到小:W2->X+>Y3+>Z2-? | |
| D. | W、X 形成的化合物中阴、阳离子个数比一定是1:2 |
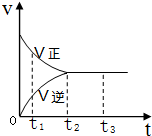 在一密闭容器中放入1mol X,进行可逆反应2X(g)?3Y(g),反应过程中的反应速率(v)与时间(t)的变化关系如图所示,下列叙述正确的是( )
在一密闭容器中放入1mol X,进行可逆反应2X(g)?3Y(g),反应过程中的反应速率(v)与时间(t)的变化关系如图所示,下列叙述正确的是( )| A. | t1时,只有正反应在进行 | |
| B. | t2~t3时间段,反应停止 | |
| C. | t2时,容器内有1.5mol Y | |
| D. | t2~t3时间段,X,Y的物质的量均没有发生变化 |
下表是一些键能数据(KJ•mol-1):
| 键能 | 键能 | 键能 | 键能 | ||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 | H-O | 464 |
| S=S | 255 | H-S | 339 | H-F | 565 | C-O | 347 |
| C-Cl | 330 | C-I | 218 | C-F | 427 |
(1)由表中数据能否得出这样的结论:①半径越小的原子形成的共价键越牢固(即键能越大)不能(填“能”或“不能”)②非金属性越强的原子形成的共价键越牢固不能(填“能”或“不能”).能否从数据找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强;试预测C-Br键的键能范围218KJ•mol-1<C-Br键能<330KJ•mol-1.
(2)已知反应H2(g)+Cl2(g)=2HCl(g)生成2mol氯化氢放热185KJ,并结合表上数据可推知一个化学反应的反应热(设反应物生成物均为气态)与反应物和生成物的键能之间的关系是化学反应的反应热等于反应物的键能之和与生成物的键能之和的差=185(KJ).
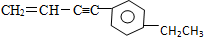 ,下列有关其结构的说法正确的是( )
,下列有关其结构的说法正确的是( )| A. | 所有碳原子可能在同一平面上 | B. | 最多有11个碳原子在同一平面上 | ||
| C. | 最多有5个碳原子在同一直线上 | D. | 最多有7个碳原子在同一直线上 |