题目内容
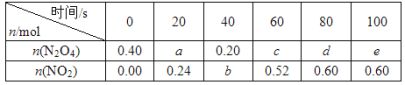
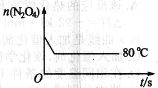
【题目】向100 mL未知浓度的AlCl3和MgCl2的混合溶液中逐滴加入0.1 mol L-1的NaOH溶液,生成沉淀的质量随加入NaOH溶液体积的变化关系如图所示。则AlCl3的浓度为

A. 0.005mol L-1 B. 0.01mol·L-1
C. 0.2mol L-1 D. 0.1mol L-1
【答案】B
【解析】根据图象可知当镁离子和铝离子完全转化为沉淀时,发生的化学反应为:2NaOH+MgCl2=2NaCl+Mg(OH)2↓、3NaOH+AlCl3=3NaCl+Al(OH)3↓,所以70mL为生成Mg(OH)2和Al(OH)3需要的NaOH溶液的体积,当沉淀最大时,继续滴加氢氧化钠溶液,发生反应NaOH+Al(OH)3=NaAlO2+2H2O,根据反应可知
NaOH+Al(OH)3=NaAlO2+2H2O
1 1
0.1mol/L×0.01L n
n=0.001mol
所以氯化铝的浓度是0.001mol÷0.1L=0.01mol/L。答案选B。

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目