题目内容
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
CH4(g)+2NO2 (g)=N2(g) + CO2(g)+2H2O(g) △H3=-867kJ·mol-1
则△H2= 。
Ⅱ.化石燃料的燃烧、含硫金属矿石的冶炼和硫酸的生产过程中产生的SO2是大气中SO2的主要来源。(1)将煤转化为水煤气是将煤转化为洁净燃料的方法之一,反应为 C(s) + H2O(g)= CO(g) + H2(g),
该反应的化学平衡常数表达式为K= 。 800℃时,将1molCO、3mol H2O、1mol H2充入容积为1L的容器中,发生反应:CO(g) + H2O(g) CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。
CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。
a加入催化剂 b降低温度 c缩小容器体积 d减少CO2的量

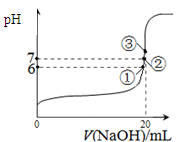
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:

①用离子方程式表示反应器中发生的反应 。
②用化学平衡移动的原理分析,在 HI分解反应中使用膜反应器分离出H2的目的是 。
Ⅲ.开发新能源是解决大气污染的有效途径之一。甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如图所示:

通入a气体的电极是原电池的 (填“正”或“负”),
其电极反应式为 。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
CH4(g)+2NO2 (g)=N2(g) + CO2(g)+2H2O(g) △H3=-867kJ·mol-1
则△H2= 。
Ⅱ.化石燃料的燃烧、含硫金属矿石的冶炼和硫酸的生产过程中产生的SO2是大气中SO2的主要来源。(1)将煤转化为水煤气是将煤转化为洁净燃料的方法之一,反应为 C(s) + H2O(g)= CO(g) + H2(g),
该反应的化学平衡常数表达式为K= 。 800℃时,将1molCO、3mol H2O、1mol H2充入容积为1L的容器中,发生反应:CO(g) + H2O(g)
 CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。
CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。a加入催化剂 b降低温度 c缩小容器体积 d减少CO2的量

(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:

①用离子方程式表示反应器中发生的反应 。
②用化学平衡移动的原理分析,在 HI分解反应中使用膜反应器分离出H2的目的是 。
Ⅲ.开发新能源是解决大气污染的有效途径之一。甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如图所示:

通入a气体的电极是原电池的 (填“正”或“负”),
其电极反应式为 。
I.-1160kJ·mol-1(2分)
II.(1)K=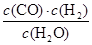 (2分) 右 (2分) b (2分)
(2分) 右 (2分) b (2分)
(2)①SO2+2H2O=H2SO4+H2 (2分) ②降低生成物的浓度,使平衡向正方向移动(2分)
Ⅲ.负(1分) CH3OH﹣6e-+H2O→CO2+6H+(2分)
II.(1)K=
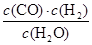 (2分) 右 (2分) b (2分)
(2分) 右 (2分) b (2分) (2)①SO2+2H2O=H2SO4+H2 (2分) ②降低生成物的浓度,使平衡向正方向移动(2分)
Ⅲ.负(1分) CH3OH﹣6e-+H2O→CO2+6H+(2分)
试题分析:Ⅰ.根据已知反应①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ·mol-1、
②CH4(g)+2NO2 (g)=N2(g) + CO2(g)+2H2O(g) △H3=-867kJ·mol-1可知,依据盖斯定律计算②×2-①即得到反应CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g),所以该反应的反应热△H2=-867kJ·mol-1×2+574kJ·mol-1=-1160kJ·mol-1。
Ⅱ.(1)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应的方程式C(s) + H2O(g)= CO(g) + H2(g)可知,该反应的平衡常数K=
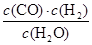 。
。(2)①t1时CO、H2O、CO2、H2的浓度(mol/L)分别是0.4、2.4、0.6、1.6,则该反应的平衡常数K=
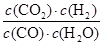 =
=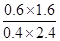 =1。t2时再向容器中充入CO、H2各1mol,此时CO、H2O、CO2、H2的浓度(mol/L)分别是1.4、2.4、0.6、2.6,则
=1。t2时再向容器中充入CO、H2各1mol,此时CO、H2O、CO2、H2的浓度(mol/L)分别是1.4、2.4、0.6、2.6,则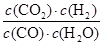 =
=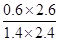 =0.46<1,所以反应向正反应方向移动,即向右移动;根据图像可知,t2时生成物浓度逐渐减小,反应物浓度逐渐增大。由于正方应是体积不变的、吸热的可逆反应,所以改变的条件应该是降低温度,导致平衡向逆反应方向移动,答案选b。
=0.46<1,所以反应向正反应方向移动,即向右移动;根据图像可知,t2时生成物浓度逐渐减小,反应物浓度逐渐增大。由于正方应是体积不变的、吸热的可逆反应,所以改变的条件应该是降低温度,导致平衡向逆反应方向移动,答案选b。(2①根据流程图可知,SO2首先被单质碘氧化,生成硫酸和碘化氢,碘化氢分解又生成单质碘和氢气,所以反应器中发生的反应的离子方程式可表示为SO2+2H2O=H2SO4+H2。
②碘化氢分解反应是可逆反应,分离出单质氢气,降低生成物的浓度,使平衡向正反应方向移动。
Ⅲ.原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。根据装置图可知,电子从左侧流向右侧,这说明左侧是负极,右侧是正极。所以通入a气体的电极是原电池的负极,通入的是甲醇。由于存在质子交换膜,因此负极电极反应式是CH3OH﹣6e-+H2O→CO2+6H+。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 ×△H 2+
×△H 2+ 2NH3(g)ΔH=-92.2kJ·mol-1
2NH3(g)ΔH=-92.2kJ·mol-1
 CO2(g)+2H2O(l) ΔH1=-Q1
CO2(g)+2H2O(l) ΔH1=-Q1 4PCl3(g) + a kJ, P4(s)+10Cl2(g)
4PCl3(g) + a kJ, P4(s)+10Cl2(g)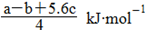

 CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为: O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
 N2(g)+2CO2(g) △H=-a kJ·mol-1。
N2(g)+2CO2(g) △H=-a kJ·mol-1。
 CO(g) + 3H2(g) △H=+206.2 kJ·mol-1
CO(g) + 3H2(g) △H=+206.2 kJ·mol-1 CO(g) + 3H2(g) ΔH>0
CO(g) + 3H2(g) ΔH>0