题目内容
(14分)无水AlCl3易升华,可用作有机合成的催化剂等。工业 上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
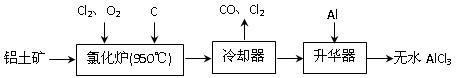
(1)氯化炉中Al2O3、C12和C反应的化学方程式为 ▲ 。
(2)用Na2SO3溶液可除去冷却器排出尾气中的Cl2,此反应的离子方程式为 ▲ 。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是 ▲ 。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3) 的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
①写出除杂过程中涉及的离子方程式 ▲ 、 ▲ 。
②AlCl3产品的纯度为 ▲ 。
(5)工业上另一种由铝灰为原料制备无水AlCl3工艺中,最后一步是由AlCl3·6H2O脱水制备无水AlCl3,实现这一步的方法是 ▲ 。
 上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
(1)氯化炉中Al2O3、C12和C反应的化学方程式为 ▲ 。
(2)用Na2SO3溶液可除去冷却器排出尾气中的Cl2,此反应的离子方程式为 ▲ 。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是 ▲ 。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3)
 的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。①写出除杂过程中涉及的离子方程式 ▲ 、 ▲ 。
②AlCl3产品的纯度为 ▲ 。
(5)工业上另一种由铝灰为原料制备无水AlCl3工艺中,最后一步是由AlCl3·6H2O脱水制备无水AlCl3,实现这一步的方法是 ▲ 。

略

练习册系列答案
相关题目
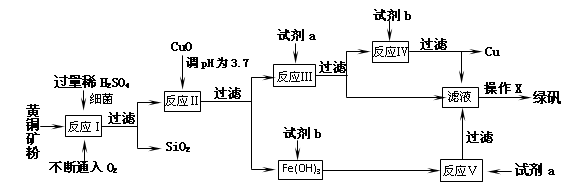
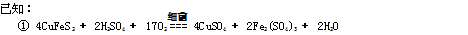
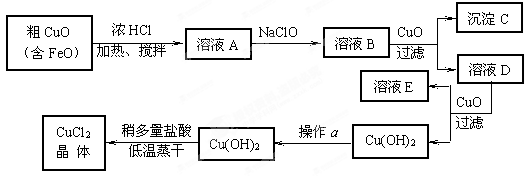
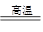 2Fe+Al2O3.这种金属冶炼的方法属于
2Fe+Al2O3.这种金属冶炼的方法属于
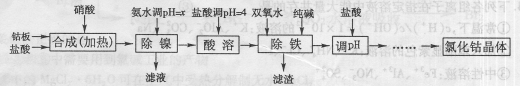
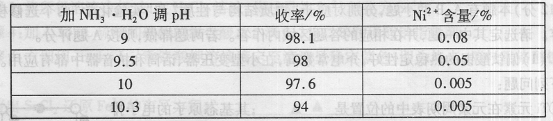
 Fe(OH)3+3H+的平衡常数为 。
Fe(OH)3+3H+的平衡常数为 。 MgO + H2O
MgO + H2O  Mg + Cl2↑
Mg + Cl2↑