��Ŀ����
��14�֣��Ի�ͭ����Ҫ�ɷ�ΪCuFeS2������������SiO2�ȣ�Ϊԭ�ϣ�����������ͭ��ͬʱ�õ�����Ʒ�̷���FeSO4��7H2O��������Ҫ�������£�
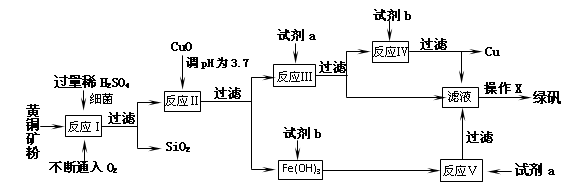
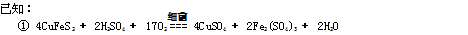
�� ����������������������ʽ��ʼ��������ȫ����ʱ��Һ��pH���±�
��1���Լ�a�� ���Լ�b�� ���ѧʽ����
��2������X��������Ϊ����Ũ���� �����ˡ�ϴ�Ӹ��
��3����Ӧ���м�CuO��pHΪ3.7��Ŀ���� ��
��4����Ӧ�������ӷ���ʽΪ ��
��5����Ӧ���У�ÿ����1mol Fe2(SO4)3��ת�Ƶ��ӵ����ʵ���Ϊ mol��
��6�����˲����У�Ҫ�õ��IJ��������� �� ��©����

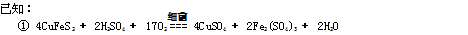
�� ����������������������ʽ��ʼ��������ȫ����ʱ��Һ��pH���±�
| ������ | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| ��ʼ����pH | 4.7 | 2.7 | 7.6 |
| ��ȫ����pH | 6.7 | 3.7 | 9.6 |
��1���Լ�a�� ���Լ�b�� ���ѧʽ����
��2������X��������Ϊ����Ũ���� �����ˡ�ϴ�Ӹ��
��3����Ӧ���м�CuO��pHΪ3.7��Ŀ���� ��
��4����Ӧ�������ӷ���ʽΪ ��
��5����Ӧ���У�ÿ����1mol Fe2(SO4)3��ת�Ƶ��ӵ����ʵ���Ϊ mol��
��6�����˲����У�Ҫ�õ��IJ��������� �� ��©����
��1�� Fe ϡ���� ��ÿ��2�֣���4�֣� ��2�� ��ȴ�ᾧ��2�֣�
��3�� ʹFe3���γ�Fe(OH)3������ͬʱ��ֹ����Cu(OH)2������2�֣�������Ҳ���֣�
��4�� Fe��2Fe3�� = 3Fe2����2�֣� ��5�� 34��2�֣�
��6�� �ձ� �� ������ ��2�֣�
��3�� ʹFe3���γ�Fe(OH)3������ͬʱ��ֹ����Cu(OH)2������2�֣�������Ҳ���֣�
��4�� Fe��2Fe3�� = 3Fe2����2�֣� ��5�� 34��2�֣�
��6�� �ձ� �� ������ ��2�֣�
�������ʵķ��뼰�ᴿ
��۾���ӦI���õ�CuSO4��Fe2(SO4)3��Һ��������ˮ��SiO2�����˺�����Һ�м���CuO�����������ᣬ�������ԣ�����pH��Fe3��ȫ��ˮ�������ȫ��
���˺���Һ������ΪCuSO4��Ϊ���յõ�ͭ���Լ�aΪ����������Fe��Cu2��=Fe2����Cu�����˺�õ�FeSO4��Һ����������ͭ�����ٽ����������Լ�b����ϡ������Fe��2H��=Fe2����H2�����õ�ͭ�ۣ�
������ӦII���˺�����Fe(OH)3����ϡ������Fe(OH)3��3H��=Fe3����2H2O���ټ�������2Fe3����Fe=3Fe2����Ҳ�ɵõ�FeSO4��Һ
����ӦIII��IV��V��ͬ���õ���FeSO4��Һ�����нᾧ���ɵõ�FeSO4����
��1���Լ�a�����ۣ��Լ�b��ϡ���ᡣ
��2����FeSO4��Һ����Ũ������ȴ�ᾧ����ˡ�ϴ�Ӹ�����ɵõ�FeSO4����
��3��CuO������Һ���������ԣ�����pH��ʹFe3��ȫ��ˮ�������ȫ��ͬʱ���ɷ�ֹ����Cu(OH)2����
��4��Fe��2Fe3�� = 3Fe2��
��5����Ӧ���У������ϼ���+2����+3��������е��ϼ��ɡ�2����+6��������4��17�ۣ�����������Ԫ�صĻ��ϼ���0�۽�����2�ۣ�������17��4�ۣ�
�ɷ���ʽ��֪��ÿ����2mol Fe2(SO4)3��ת�Ƶ��ӵ����ʵ���Ϊ68mol���ʴ�Ϊ34
��6�����˲����У�Ҫ�õ��IJ����������ձ� �� ��������©����
��۾���ӦI���õ�CuSO4��Fe2(SO4)3��Һ��������ˮ��SiO2�����˺�����Һ�м���CuO�����������ᣬ�������ԣ�����pH��Fe3��ȫ��ˮ�������ȫ��
���˺���Һ������ΪCuSO4��Ϊ���յõ�ͭ���Լ�aΪ����������Fe��Cu2��=Fe2����Cu�����˺�õ�FeSO4��Һ����������ͭ�����ٽ����������Լ�b����ϡ������Fe��2H��=Fe2����H2�����õ�ͭ�ۣ�
������ӦII���˺�����Fe(OH)3����ϡ������Fe(OH)3��3H��=Fe3����2H2O���ټ�������2Fe3����Fe=3Fe2����Ҳ�ɵõ�FeSO4��Һ
����ӦIII��IV��V��ͬ���õ���FeSO4��Һ�����нᾧ���ɵõ�FeSO4����
��1���Լ�a�����ۣ��Լ�b��ϡ���ᡣ
��2����FeSO4��Һ����Ũ������ȴ�ᾧ����ˡ�ϴ�Ӹ�����ɵõ�FeSO4����
��3��CuO������Һ���������ԣ�����pH��ʹFe3��ȫ��ˮ�������ȫ��ͬʱ���ɷ�ֹ����Cu(OH)2����
��4��Fe��2Fe3�� = 3Fe2��
��5����Ӧ���У������ϼ���+2����+3��������е��ϼ��ɡ�2����+6��������4��17�ۣ�����������Ԫ�صĻ��ϼ���0�۽�����2�ۣ�������17��4�ۣ�
�ɷ���ʽ��֪��ÿ����2mol Fe2(SO4)3��ת�Ƶ��ӵ����ʵ���Ϊ68mol���ʴ�Ϊ34
��6�����˲����У�Ҫ�õ��IJ����������ձ� �� ��������©����

��ϰ��ϵ�д�
�����Ŀ

 ����
���� ��
��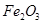 ��MgO�����ʣ�����ȡAl2O3�����ֹ���Ʒ�������£�
��MgO�����ʣ�����ȡAl2O3�����ֹ���Ʒ�������£�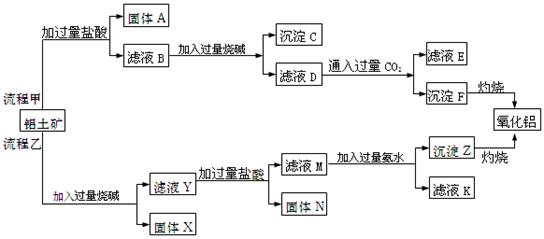



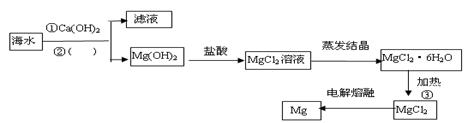
 ����������A12O3��Fe2O3��Ϊԭ���Ʊ���ˮAlCl3�Ĺ����������¡�
����������A12O3��Fe2O3��Ϊԭ���Ʊ���ˮAlCl3�Ĺ����������¡�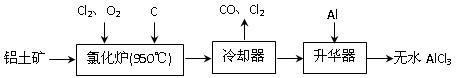
 �Ĵ��ȣ���ȡ16.25 g��ˮAlCl3��Ʒ�����ڹ�����NaOH��Һ�����˳�����������ᆳϴ�ӡ����ա���ȴ�����أ�������������Ϊ0.32 g��
�Ĵ��ȣ���ȡ16.25 g��ˮAlCl3��Ʒ�����ڹ�����NaOH��Һ�����˳�����������ᆳϴ�ӡ����ա���ȴ�����أ�������������Ϊ0.32 g��