题目内容
【题目】800℃时,在2L密闭容器中发生反应2NO(g)+O2(g)2NO2(g),在反应体系中,n(NO)随时间的变化如表所示:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
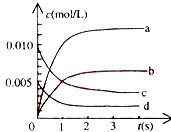
①图中表示NO2变化的曲线是 , 用O2表示从0~2s内该反应的平均速率v= .
②能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变.
【答案】b;0.0015mol/(L?s);bc
【解析】解:①从图象分析,随反应时间的延长,各物质的浓度不再不变,且反应物没有完全反应,所以反应为可逆反应,根据一氧化氮物质的量的变化知,该反应向正反应方向移动,则二氧化氮的物质的量在不断增大,且同一时间段内,一氧化氮减少的物质的量等于二氧化氮增加的物质的量,所以表示NO2的变化的曲线是b,
0~2s内v(NO)= ![]() =0.0030mol/(L.min),同一化学反应同一时间段内,各物质的反应速率之比等于其计量数之比,所以氧气的反应速率为 0.0015mol/(Ls),
=0.0030mol/(L.min),同一化学反应同一时间段内,各物质的反应速率之比等于其计量数之比,所以氧气的反应速率为 0.0015mol/(Ls),
所以答案是:b,0.0015mol/(Ls); ②a.反应速率之比等于化学方程式计量数之比,v(NO2)=2v(O2)为正反应速率之比,不能说明正逆反应速率相同,无法判断正逆反应速率是否相等,故a错误;
b.反应前后气体体积不同,压强不变说明正逆反应速率相等,各组分浓度不变,故b正确;
c.反应速率之比等于化学方程式计量数之比为正反应速率之比,v逆(NO)=2v正(O2)时,一氧化氮正逆反应速率相同,说明反应达到平衡状态,故c正确;
d.恒容容器,反应物生成物都是气体质量不变,体积不变,所以密度始终不变,不能说明反应达到平衡状态,故d错误;
故选bc,
所以答案是:bc.
【考点精析】认真审题,首先需要了解化学平衡状态的判断(状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等).

 名校课堂系列答案
名校课堂系列答案