题目内容
【题目】已知A、B、C均为气体,在体积为10L的恒容密闭容器中进行发生可逆反应,在0~3分钟内各物质的量的变化情况如图所示.请回答下列问题: 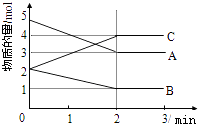
①反应开始至2分钟时,B的平均反应速率为 .
②该反应的化学反应方程式为
③由图求3min时A的转化率为 .
【答案】0.05mol/(L.min);2A+B?2C;40%
【解析】解:①由图象可以看出,反应开始至2分钟时,△n(B)=1mol,B的平均反应速率= ![]() =0.05mol/(L.min),
=0.05mol/(L.min),
所以答案是:0.05mol/(L.min);②由图象可以看出,A、B的物质的量逐渐减小,则A、B为反应物,C的物质的量逐渐增多,所以C为生成物,当反应到达2min时,△n(A)=2mol,△n(B)=1mol,△n(C)=2mol,化学反应中,各物质的物质的量的变化值与化学计量数呈正比,则△n(A):△n(B):△n(C)=2:1:2,所以反应的化学方程式为:2A+B2C,
所以答案是:2A+B2C;③由图可知:达平衡时,△n(A)=2mol,所以A的转化率为 ![]() ×100%=40%,
×100%=40%,
所以答案是:40%.
【考点精析】解答此题的关键在于理解反应速率的定量表示方法的相关知识,掌握反应速率的单位:mol/(L·min)或mol/(L·s) v=△c-△t,以及对化学平衡的计算的理解,了解反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.

 阅读快车系列答案
阅读快车系列答案【题目】800℃时,在2L密闭容器中发生反应2NO(g)+O2(g)2NO2(g),在反应体系中,n(NO)随时间的变化如表所示:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
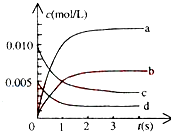
①图中表示NO2变化的曲线是 , 用O2表示从0~2s内该反应的平均速率v= .
②能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变.