题目内容
【题目】固体粉末X中可能含有K2SO3、K2CO3、FeO、Fe2O3、MnO2、Na2SO4、NaNO3中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下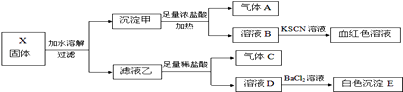
根据上述实验,下列说法正确的是 ( )
A.固体X中一定含有Fe2O3
B.沉淀E可能含有BaSO3
C.气体A,C一定均为纯净物
D.固体X可能出现含有K2SO3、K2CO3而不含Na2SO4的情况
【答案】D
【解析】根据流程图,沉淀甲可能含有FeO、Fe2O3、MnO2 , 加入足量的浓盐酸加热,有气体A生成,说明气体A是氯气,甲中含有MnO2 , 溶液B中加入KSCN后也会出现血红色溶液,溶液B中一定含有铁离子,由于反应中生成了氯气,因此铁离子可能来自于FeO或Fe2O3 ,固体X不一定含有Fe2O3 ;B.滤液乙中可能含有K2SO3、K2CO3、Na2SO4、NaNO3 , 加入足量稀盐酸,生成气体C,气体C可能是二氧化碳或二氧化硫或两者的混合物,溶液D中可能含有Na2SO4、NaNO3 , 加入BaCl2溶液,生成白色沉淀,则沉淀一定是BaSO4沉淀,说明溶液D中一定含有Na2SO4 , Na2SO4可能来自于亚硫酸钠在酸性条件下被NaNO3氧化而来,根据上述分析,答案选D。根据常见离子的检验方法和实验现象判断操作过程中物质的存在情况即可。

练习册系列答案
相关题目