��Ŀ����
����Ŀ��I��25��ʱ�������ΪVa��pH��a��ijһԪǿ����Һ�����ΪVb��pH��b��ijһԪǿ����Һ��ϣ�ǡ���к͡���ش�
����a��b��12����Va��Vb��________��
����Va��Vb��a��0.5b����a��ȡֵ��Χ��_________________��
II�����ӹ�ҵ�У�����FeCl3��Һ��Ϊӡˢ��·ͭ��ʴ��Һ��ij̽��С�����������·������Һ����Դ���գ�
��ش�

(1)��������FeCl3��Һʴ��ͭ���ķ�Һ�к��еĽ�����������_____________��
(2)������м���H2O2��Һ��Ŀ����________________________________________��
(3)��֪�������������������pH
Cu(OH) 2 | Fe(OH) 2 | Fe(OH) 3 | |
��ʼ����ʱ | 4.7 | 7.0 | 1.9 |
������ȫʱ | 6.7 | 9.0 | 3.2 |
���ݱ��������Ʋ����pH�ķ�Χ��_____________��
(4)��Ҫ��ȥ����MgCl2��Һ�е�FeCl3������Լ�����Լ���_____________��(����ĸ)
A��NaOH B��Mg(OH)2 C��MgCO3 D�� NH3H2O
���𰸡�1��100 7/2<a<14/3 Fe3+��Fe2+��Cu2+ ��Fe2+������Fe3+���Ա����ת��ΪFe(OH)3������ȥ 3.2��pH��4.7 BC
��������
I�����ΪVa��pH=a��ijһԪǿ�������Vb��pH=b��ijһԪǿ���ϣ�ǡ���кͣ�����Va10-a=Vb10b-14���ݴ˷���������жϣ�
II��FeCl3��Һʴ��ͭ���ķ�Һ������2Fe3++Cu=2Fe2++Cu2+���õ��Ȼ�ͭ���Ȼ��������Ȼ����Ļ����Һ�����Һ�е���������⽫�������������ɼ��׳�ȥ�������ӣ�Ȼ�������Һ��pH�����˵ó��������������Ȼ�ͭ��Һ���������ܽ�������õ��Ȼ���������Һ�м���̼�����Ƶõ���ʽ̼��ͭ���ݴ˷������
I�����ΪVa��pH=a��ijһԪǿ�������Vb��pH=b��ijһԪǿ���ϣ�ǡ���кͣ�����Va10-a=Vb10b-14��
��a��b��12ʱ��![]() ��10(a+b14)= 102=
��10(a+b14)= 102=![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��![]() ��
��![]() ��
��![]() ��10(a+b14)��1������(a+b-14)��0����a=0.5b����3a��14��a��
��10(a+b14)��1������(a+b-14)��0����a=0.5b����3a��14��a��![]() ����pH=b=2a��7��a��
����pH=b=2a��7��a��![]() ������
������![]() ��a��
��a��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��a��
��a��![]() ��
��
II��(1)�Ȼ�����ͭ��Ӧ�����Ȼ��������Ȼ�ͭ����Ӧ�����ӷ���ʽ��2Fe3++Cu=2Fe2++Cu2+�������ӿ��ܹ������ʴ�Ϊ��Fe3+��Fe2+��Cu2+��
(2)������������������������Ϊ�����ӵ����������µ����ʣ�������ѡ��������⣬�����������ӵ����ӷ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O���ʴ�Ϊ����Fe2+������Fe3+���������ת��ΪFe(OH)3������ȥ��
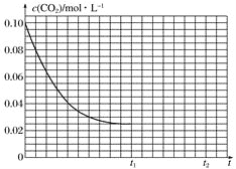
(3)������Һ��pHĿ����ʹ������ȫ��������ͭ���Ӳ�����������ͼ�����ݷ�����֪pHӦΪ��3.2��4.7���ʴ�Ϊ��3.2��pH��4.7��
(4)�Ȼ�����ˮ����������������ϡ���ᣬҪ��ȥMgCl2������Һ��������FeCl3����������ʲ��������������ܺ��Ȼ�����ϡ���ᷴӦ��MgO��Mg(OH)2��MgCO3�����Ժ��ᷴӦ�����Ȼ�þ��������Һ���ԣ��ٽ�������ˮ������ɳ�������������������ƺͰ�ˮ������������ӣ���ѡBC��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�