题目内容
【题目】下列实验能达到实验目的的是( )
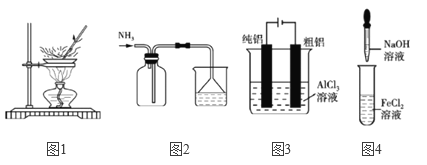
A. 用图1装置将硫酸铜溶液直接蒸干得到胆矾 B. 图2装置可用于收集氨气并进行尾气吸收
C. 用图3装置电解精炼铝 D. 图4装置可以用于实验室制备Fe(OH)2
【答案】B
【解析】A.用图1装置将硫酸铜溶液直接蒸干得到的为硫酸铜,不是胆矾,故错误;B. 氨气的密度比空气小,用向下排空气法收集,氨气极易溶于水,所以可以用水吸收尾气,使用倒置漏斗可以防止倒吸,所以图2装置可用于收集氨气并进行尾气吸收,故正确;C.电解精炼铝时应该将粗铝连接电源的正极,纯铝连接电源的负极,故用图3装置不能电解精炼铝,故错误; D.实验室制备Fe(OH)2时应该将盛有氢氧化钠溶液的胶头滴管伸入到液面以下再挤出氢氧化钠,避免反应生成的氢氧化亚铁与空气接触而反应,故图4装置错误。故选B。

练习册系列答案
相关题目