题目内容
【题目】现有短周期元素A、B、C、D。A元素M层上有2对成对电子,D与A在周期表中同一主族。由A、B与D组成的化合物的浓溶液是常见的干燥剂,常温下C单质为双原子分子,其氢化物水溶液呈碱性,是一种重要的肥料。
完成下列填空。
(1)A的原子最外层电子排布式为______,该电子层内含______种不同运动状态的电子。描述集气瓶中足量的A的氢化物与其低价态氧化物混合后,充分反应的实验现象:______。
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,其化学式是______。写出该化合物在实验室制备乙酸乙酯时所起的作用:______。
(3)B与C元素形成带一个单位正电荷的离子,写出该微粒的电子式___。写出实验室检验溶液中该离子的简单实验方案:_______。
(4)元素A与元素D相比,非金属性较强的是______(用元素符号表示),下列表述中能表明这一事实的是_______。
①比较最高价氧化物对应水化物的酸性
②比较对应气态氢化物的稳定性
③一定条件下D能从A的氢化物水溶液中置换出A单质
④A单质的熔沸点明显高于D单质
(5)C的氢化物固态时属于________晶体,该氢化物与少量A的最高价氧化物水化物反应的化学方程式是________。
【答案】3s23p4 6 有淡黄色粉末和无色液体生成 H2SO4 催化、吸水 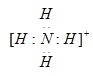 取适量待测液于试管中,加入适量NaOH溶液后加热,若产生无色有刺激性气味的气体,且能使试管口湿润的红色石蕊试纸变蓝,则证明溶液中含有铵根离子 O ②③ 分子 H2SO4+2NH3=(NH4)2SO4
取适量待测液于试管中,加入适量NaOH溶液后加热,若产生无色有刺激性气味的气体,且能使试管口湿润的红色石蕊试纸变蓝,则证明溶液中含有铵根离子 O ②③ 分子 H2SO4+2NH3=(NH4)2SO4
【解析】
现有短周期元素A、B、C、D,A元素M层上有2对成对电子,则A的M层含有6个电子,为S元素;D与A在周期表中同一主族,则D为O元素;由A、B与D组成的化合物的浓溶液是常见的干燥剂,该干燥剂为浓硫酸,则B为H元素;常温下C单质为双原子分子,其氢化物水溶液呈碱性,是一种重要的肥料,则C为N元素,据此结合元素周期律知识进行解答。
根据上述分析可知A是S元素,B是H元素,C是N元素,D是O元素;
(1)A为S元素,S原子的最外层含有6个电子,A的原子最外层电子排布式为3s23p4,最外层共有6种不同运动状态的电子;A的氢化物为H2S,S的低价态氧化物为SO2,H2S与SO2混合后生成硫单质和水,因此反应现象为:有淡黄色粉末和无色液体生成;
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,该干燥剂为浓H2SO4,在实验室中用乙醇和乙酸及浓硫酸混合加热,发生酯化反应产生乙酸乙酯和水,在制备乙酸乙酯中浓硫酸为催化剂和吸水剂;
(3)B与C元素形成带一个单位正电荷的离子,该离子为NH4+,其电子式为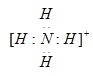 ,在实验室中检验NH4+的方法为:取适量待测液于试管中,加入适量NaOH溶液后加热,若产生无色有刺激性气味的气体,且能使试管口湿润的红色石蕊试纸变蓝,则证明溶液中含有铵根离子;
,在实验室中检验NH4+的方法为:取适量待测液于试管中,加入适量NaOH溶液后加热,若产生无色有刺激性气味的气体,且能使试管口湿润的红色石蕊试纸变蓝,则证明溶液中含有铵根离子;
(4)元素S与元素O相比,二者位于同一主族,由于原子序数越大,原子核外电子层数越多,原子半径越大,元素的非金属性越弱,因此元素的非金属性较强的是O元素;
①O元素没有含氧酸,无法据此判断非金属性强弱,①错误;
②元素的氢化物稳定性越强,说明该元素与H元素的原子结合力越强,则元素的非金属性就越强,因此可通过比较对应气态氢化物的稳定性,可以判断二者非金属性强弱,②正确;
③一定条件下氧气能从硫化氢的水溶液中置换出S单质,从而证明O的非金属性大于O,③正确;
④沸点大小与非金属性没有必然关系,无法根据沸点高低判断非金属性强弱,④错误;
故合理选项是②③;
(5)C为N元素,其氢化物为氨气,氨气是由分子构成的物质,在固态时属于分子晶体;A的最高价氧化物水化物为硫酸,氨气与硫酸发生反应产生硫酸铵,反应的化学方程式为:H2SO4+2NH3=(NH4)2SO4。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案