题目内容
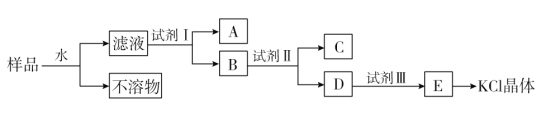
【题目】软锰矿是一种常见的锰矿物,主要成分是MnO2,常含有铁、铝元素形成的杂质。工业上,用软锰矿制取高锰酸钾的流程如下(部分条件和产物省略)

请回答下列问题
(1)在“水浸”过程中,提高K2MnO4浸出率(浸出的K2MnO4质量与“熔块”质量之比)的措施有____________________________________________(至少写出两点)
(2)“熔融”过程中发生的主要反应其化学方程式为_________________________________。
(3)CO2与K2MnO4反应的离子方程式为_________________________________。
(4)KMnO4与K2CO3能用重结晶的方法分离的原理是______________________。
(5)“电解”过程中使用的是惰性电极,则:
①阳极的电极反应方程式为______________________。
②阴极附近溶液的pH将___________(填“增大”、“减小”或“不变”)
(6)可用过氧化氢溶液滴定的方法测定高锰酸钾样品纯度。当达到滴定终点时,溶液中产生的现象为_________________________________。
(7)在上述生产过程中产生的M2+会对环境造成污染。工业上,通过调节pH使废水中的Mn2+形成Mn(OH)2沉淀。当pH=10时,溶液中的c(Mn2+)=___________mol/L(已知:Ksp[Mn(OH)2]=2.0×10-13。相关数据均在常温下测定)
【答案】将“熔块”粉碎、加热、用玻璃棒搅拌等 2MnO2+O2+4KOH △ 2K2MnO4+2H2O 3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32- 随温度的改变,KMnO4与K2CO3的溶解度变化量差别较大 MnO42--e-=MnO4- 增大 当加入最后1滴过氧化氢溶液时,由紫红色刚好褪色且半分钟内不变色 2.0×10-5
【解析】
软锰矿的主要成分是MnO2,由工艺流程转化关系可知,MnO2、KOH的熔融混合物中通入空气时发生反应生成K2MnO4,向K2MnO4溶液中通入CO2制备KMnO4,还生成K2CO3、MnO2,通过过滤,分离出二氧化锰,滤液中含KMnO4和K2CO3,根据KMnO4和K2CO3在溶解性上不同采用蒸发结晶的方式可分离出高锰酸钾和碳酸钾,对粗高锰酸钾进行重结晶、干燥得到纯净的高锰酸钾。
(1)为提高提高锰酸钾浸出率,应采用加热、搅拌的方法,使反应尽可能多的生成锰酸钾;
故答案为:将“熔块”粉碎、加热、用玻璃棒搅拌等;
(2)根据流程图,二氧化锰与氢氧化钾溶液、氧气在高温条件下发生反应生成锰酸钾和水,化学方程式为2MnO2+O2+4KOH △ 2K2MnO4+2H2O;
故答案为:2MnO2+O2+4KOH △ 2K2MnO4+2H2O;
(3)由流程可知,CO2与K2MnO4反应生成KMnO4,还生成K2CO3、MnO2,所以反应的离子方程式为3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-;
故答案为:3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-;
(4)根据KMnO4和K2CO3在溶解性上不同采用蒸发结晶的方式可分离出高锰酸钾和碳酸钾,故KMnO4与K2CO3能用重结晶的方法分离的原理是随温度的改变,KMnO4与K2CO3的溶解度变化量差别较大;
故答案为:随温度的改变,KMnO4与K2CO3的溶解度变化量差别较大;
(5)锰酸钾生成高锰酸钾,Mn元素的化合价升高,所以锰酸钾发生氧化反应,所以电解锰酸钾溶液的阳极反应式为锰酸根离子失去电子生成高锰酸根离子,电极反应式为MnO42--e-=MnO4-;阴极是氢离子放电生成氢气,氢离子浓度减小,氢氧根离子浓度增大,则溶液的pH增大;
故答案为:MnO42--e-=MnO4- ;增大;
(6)用过氧化氢溶液滴定高锰酸钾溶液,当达到滴定终点时,高锰酸钾被还原,故溶液中产生的现象为当加入最后1滴过氧化氢溶液时,由紫红色刚好褪色且半分钟内不变色;
故答案为:当加入最后1滴过氧化氢溶液时,由紫红色刚好褪色且半分钟内不变色;
(7)Mn(OH)2的溶度积Ksp=c(Mn2+)c2(OH-)=2.0×10-13,当pH=10时,c(OH-)=1.0×10-4mol/L,所以c(Mn2+)=2.0×10-13/ c2(OH-)=![]() mol/L =2.0×10-5mol/L。
mol/L =2.0×10-5mol/L。
故答案为:2.0×10-5。