题目内容
4.同时加热氯化镁晶体(MgCl2•6H2O)和硫酸镁晶体(MgSO4•7H2O)时,氯化镁易发生水解反应,其原因是( )| A. | 硫酸镁晶体分解反应是放热反应 | B. | 氯化镁水解是熵增反应 | ||
| C. | 硫酸镁晶体分解反应是熵减反应 | D. | 氯化镁分解放热比硫酸镁少 |
分析 MgCl2•6H2O水解生成的HCl易挥发,使水解平衡正移,MgSO4•7H2O水解生成的H2SO4难挥发,据此分析.
解答 解:已知MgCl2•6H2O受热时发水解:MgCl2•6H2O═Mg(OH)Cl+HCl↑+5H2O,MgCl2•6H2O水解生成的HCl易挥发,使水解平衡正移,导致水解容易进行,MgSO4•7H2O水解生成的H2SO4难挥发,H2SO4会抑制MgSO4•7H2O水解,所以MgSO4•7H2O受热不易发生水解,由于MgCl2水解生成挥发性酸HCl,在加热时,以HCl气体形式逸出,熵增加.
故选B.
点评 本题考查了水解平衡移动,题目难度不大,侧重于基础知识的考查,注意水解产物对水解反应的影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.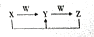 A、B、C、D、E均是常见短周期元素,其在周期表中的位置如图.
A、B、C、D、E均是常见短周期元素,其在周期表中的位置如图.
(1)D的元素符号为O,常用于测定文物年代的同位素是146C.
(2)A与C可形成多种10电子微粒,其中分子为NH3,离子为NH4+.
(3)C、D、E的简单离子的半径大小顺序为N3->O2->Na+;
(4)A与C可形成两种常见的化合物,化合物P(相对分子质量为17)和化合物Q(相对分子质量为32).
①写出Q的结构式: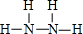
②P的水溶液可作腐蚀剂H2O2的消除剂,其反应物不污染环境,其化学方程式为2NH3.H2O+3H2O2=N2↑+8H2O.
(5)由A、B、C、D、E四种元素中的二种或二种以上元素组成的化合物X、Y、Z、W有如下转化关系: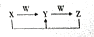 ,其中Y和Z在水溶液中存在的微粒种类相同.
,其中Y和Z在水溶液中存在的微粒种类相同.
①X化合物中含有的化学键类型有离子键、共价键.
②反应X+Z→Y的离子方程式为HCO3-+OH-=CO32-+H2O.
③Y的水溶液中离子浓度的大小顺序是c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
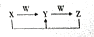 A、B、C、D、E均是常见短周期元素,其在周期表中的位置如图.
A、B、C、D、E均是常见短周期元素,其在周期表中的位置如图. | A | |||||
| B | C | D | |||
| E | |||||
(2)A与C可形成多种10电子微粒,其中分子为NH3,离子为NH4+.
(3)C、D、E的简单离子的半径大小顺序为N3->O2->Na+;
(4)A与C可形成两种常见的化合物,化合物P(相对分子质量为17)和化合物Q(相对分子质量为32).
①写出Q的结构式:
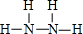
②P的水溶液可作腐蚀剂H2O2的消除剂,其反应物不污染环境,其化学方程式为2NH3.H2O+3H2O2=N2↑+8H2O.
(5)由A、B、C、D、E四种元素中的二种或二种以上元素组成的化合物X、Y、Z、W有如下转化关系:
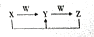 ,其中Y和Z在水溶液中存在的微粒种类相同.
,其中Y和Z在水溶液中存在的微粒种类相同.①X化合物中含有的化学键类型有离子键、共价键.
②反应X+Z→Y的离子方程式为HCO3-+OH-=CO32-+H2O.
③Y的水溶液中离子浓度的大小顺序是c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
15.已知某温度下,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1.12×10-12,下列叙述正确的是( )
| A. | 向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp减小 | |
| B. | 向2.0×10-4 mol/L的K2CrO4溶液中加入等体积的2.0×10-4mol/AgNO3溶液后,则有Ag2CrO4沉淀生成 | |
| C. | 将一定量的AgCl和Ag2CrO4固体混合物溶于蒸馏水中,充分溶解后,静置,上层清液中的Cl的物质的量浓度最大 | |
| D. | 将0.001mol/L的AgNO3溶液逐滴滴入0.001mol/L的KCl和0.001mol/L的K2CrO4的混合溶液中,则先产生AgCl沉淀. |
12.下列有关实验操作或原理正确的是( )
| A. | 取少量硫酸亚铁铵品体溶于水,先加入氯水,再滴入几滴硫氰化钾溶液,溶液变血红色,则可证明品体的成分中含有Fe2+ | |
| B. | 用到金属钠时,要用镊子取,再用小刀切下所需量,剩余钠不能放回原试剂瓶中 | |
| C. | 用pH计分别测定0.1mol•L-1的FeCl3和0.01mol•L-1FeCl3的pH,可以比较浓度对盐类水解程度的影响 | |
| D. | 通过测定等物质的量浓度的NaCl、Na2S溶液的pH,比较硫、氯两种元素的非金属性强弱 |
9.下列关于化学基本概念的认识中正确的是( )
| A. | 用H2O,C2H6表示的物质一定是纯净物 | |
| B. | 氯化钡的分子式BaCl2可以表示其组成 | |
| C. | 胶体区别于其它分散系的本质特征是丁达尔现象 | |
| D. | 质子数,中子数,电子数都相同的微粒一定是同一种粒子 |
16. 利用环境中细菌对有机质的催化降解能力,科学家开发出了微生物燃料电池,其装置如图:a、b为惰性电极.利用该装置将污水中的有机物(以C6H12O6为例)经氧化而除去,从而达到净化水的目的.下列说法不正确的是( )
利用环境中细菌对有机质的催化降解能力,科学家开发出了微生物燃料电池,其装置如图:a、b为惰性电极.利用该装置将污水中的有机物(以C6H12O6为例)经氧化而除去,从而达到净化水的目的.下列说法不正确的是( )
 利用环境中细菌对有机质的催化降解能力,科学家开发出了微生物燃料电池,其装置如图:a、b为惰性电极.利用该装置将污水中的有机物(以C6H12O6为例)经氧化而除去,从而达到净化水的目的.下列说法不正确的是( )
利用环境中细菌对有机质的催化降解能力,科学家开发出了微生物燃料电池,其装置如图:a、b为惰性电极.利用该装置将污水中的有机物(以C6H12O6为例)经氧化而除去,从而达到净化水的目的.下列说法不正确的是( )| A. | a为负极,电极反应式为:C6H12O6+6H2O-24e-═6CO2+24H+ | |
| B. | 反应过程中产生的质子透过阳离子交换膜扩散到好氧区 | |
| C. | 装置中的离子交换膜是阳离子交换膜 | |
| D. | 该装置把电能转化为生物质能 |
14.用下列装置进行相应实验,能达到实验目的是( )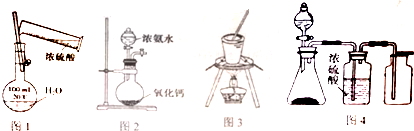

| A. | 用图1所示配制一定浓度的稀硫酸 | B. | 用图2装置实验室制取氨气 | ||
| C. | 用图3装置蒸发饱和食盐水 | D. | 用图4装置制取、收集乙炔气体 |
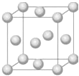 铜合金是人类使用最早的金属材料.铜在化合物中的常见化合价有+l、+2 等,故能形成多种铜的化合物.
铜合金是人类使用最早的金属材料.铜在化合物中的常见化合价有+l、+2 等,故能形成多种铜的化合物.