题目内容
2. 环己烯是一种重要的化工原料.
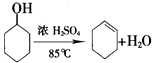
环己烯是一种重要的化工原料.(1)实验室可由环己醇制备环己烯,反应的化学方程式是
 .
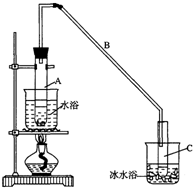
.(2)实验装置如图所示,将10mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.
环己醇和环己烯的部分物理性质如下:
| 密度 (g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
②试管A置于水浴中的目的是受热均匀,便于控温;试管C置于冰水浴中的目的是使环己烯液化,减少挥发.
(3)环己烯粗品中含有少量环己醇和酸性杂质.精制环己烯的方法是:
①向环己烯粗品中加入C(填入编号),充分振荡后,分液(填操作名称).
A.Br2的CCl4溶液 B.稀H2SO4 C.Na2CO3溶液
②再对初步除杂后的环己烯进行蒸馏,得到环己烯精品.蒸馏时,蒸馏烧瓶中要加入少量生石灰,目的是除去产品中少量的水.
③实验制得的环己烯精品质量低于理论产量,可能的原因是C.
A.蒸馏时从70℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(4)以下区分环己烯精品和粗品的方法,合理的是B.
A.加入水观察实验现象
B.加入金属钠观察实验现象
C.加入酸性高锰酸钾溶液,振荡后观察实验现象.
分析 (1)实验室用环己醇在浓硫酸加热到85℃发生消去反应制备环己烯;
(2)①根据实验室制乙烯可知,发生装置A中碎瓷片的作用是防止暴沸;导管B比较长,能增加与空气的接触面积,其作用是导气和将生成的气体物质冷凝回流;
②水浴加热能使受热均匀,且便于控制温度;冰水浴的目的是降低环己烯蒸气的温度,使其液化;
(3)①环己烯粗品中还含有少量的酸和环己醇,联想:制备乙酸乙酯提纯产物时用c(Na2CO3溶液)洗涤可除去酸,充分振荡后,再分液;
②生石灰能与水反应生成氢氧化钙,利于环己烯的蒸出;
③根据表中数据可知,馏分环己烯的沸点为83℃;
a、若提前收集,产品中混有杂质,实际产量高于理论产量;
b、制取的环己烯物质的量增大,实验制得的环己烯精品质量高于理论产量;
c、粗产品中混有环己醇,导致测定消耗的环己醇量增大,制得的环己烯精品质量低于理论产量;
(4)环己烯粗品中含有环己醇,根据环己醇能与钠产生氢气,而环己稀不能,据此选择.
解答 解:(1)实验室用环己醇在浓硫酸加热到85℃发生消去反应制备环己烯,反应的方程式为 ,
,
故答案为: ;
;
(2)①根据制乙烯实验的知识,发生装置A中碎瓷片的作用是防止暴沸,由于生成的环己烯的沸点为83℃,要得到液态环己烯,导管B除了导气外还具有冷凝作用,便于环己烯冷凝,
故答案为:防止暴沸;冷凝;
②由于制取环已烯的反应条件是85℃,所以用水浴加热,水浴加热能使受热均匀,且便于控制温度;冰水浴的目的是降低环己烯蒸气的温度,使其液化,
故答案为:受热均匀,便于控温;使环己烯液化,减少挥发;
(3)①环己烯粗品中还含有少量的酸和环己醇,环己烯中含有碳碳双键,可以被KMnO 4溶液氧化,稀H2SO4不能除去,反而能引入新的酸性杂质,只有Na2CO 3溶液,不能与环己烯反应,可以与酸性杂质反应,可选C,充分振荡后,再分液;
故答案为:C;分液;
②生石灰能与水反应生成氢氧化钙,除去了残留的水,得到纯净的环己烯,故答案为:除去产品中少量的水;
③根据表中数据可知,馏分环己烯的沸点为83℃,故收集产品应控制温度在83℃左右;
a、蒸馏时从70℃开始收集产品,提前收集,产品中混有杂质,实际产量高于理论产量,故a错误;
b、环己醇实际用量多了,制取的环己烯的物质的量增大,实验制得的环己烯精品质量高于理论产量,故b错误;
c、若粗产品中混有环己醇,导致测定消耗的环己醇量增大,制得的环己烯精品质量低于理论产量,故c正确;
故答案为:C;
(4)环己烯粗品中含有环己醇,根据环己醇能与钠产生氢气,而环己稀不能,加入水观察实验现象,环己烯精品和粗品没有区别,环己烯精品和粗品都能使高锰酸钾褪色,故选B.
点评 本题以有机合成为载体,综合考查了环己烯的制备,考查了学生运用知识的能力,题目难度中等,注意把握实验原理和方法,特别是实验的基本操作,学习中注意积累.

 阅读快车系列答案
阅读快车系列答案| A. |  金刚石模型 | B. | 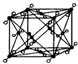 干冰模型 | C. | 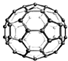 碳60模型 | D. | 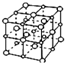 氯化钠模型 |
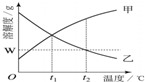 如图是甲、乙两种物质的溶解度曲线.在t2℃时向盛有100g水的烧杯中先后加入wg甲和wg乙(两种物质溶解时互不影响),充分搅拌.将混合物的温度降低到t1℃.下列说法正确的是( )
如图是甲、乙两种物质的溶解度曲线.在t2℃时向盛有100g水的烧杯中先后加入wg甲和wg乙(两种物质溶解时互不影响),充分搅拌.将混合物的温度降低到t1℃.下列说法正确的是( )| A. | 甲物质的溶解度随温度升高而减小 | |
| B. | 温度降低到t1℃时,得到甲、乙的饱和溶液 | |
| C. | 温度降低到t1℃时,甲、乙的溶质质量分数相等,得到甲、乙的不饱和溶液 | |
| D. | t2℃时,甲物质的溶液为饱和溶液,乙物质的溶液为不饱和溶液 |
| ① | 氯化铁溶液加热蒸干最终得不到氯化铁固体 | |
| ② | 镀锡的铁制品,镀层部分受损后,露出的铁表面更易被腐蚀 | |
| ③ | 电解精炼铜时,每转移2mol电子阳极上溶解的铜原子数为NA | |
| ④ | 在lL0.1mol.L-1碳酸钠溶液中,阴离子总数大于0.1NA |
| A. | ① | B. | ② | C. | ③ | D. | ④ |
 如图是实验室制取溴苯的装置,说明:
如图是实验室制取溴苯的装置,说明: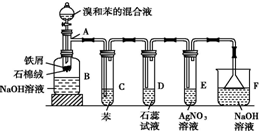 (1)苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.
(1)苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑. .
.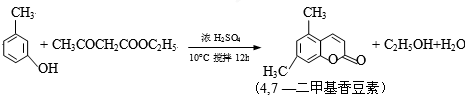
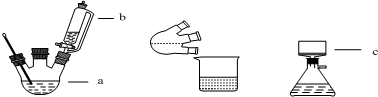
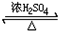 CH3COOCH2CH3+H2O,用饱和的碳酸钠溶液(填药品名称)收集粗产品,用分液(填操作名称)的方法把粗产品分离.
CH3COOCH2CH3+H2O,用饱和的碳酸钠溶液(填药品名称)收集粗产品,用分液(填操作名称)的方法把粗产品分离.