题目内容
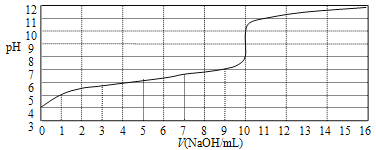
【题目】以0.10mol/L的氢氧化钠溶液滴定某一元弱酸(已知其在该条件下的电离度α≈1%)的滴定曲线如图所示。横坐标为加入氢氧化钠的体积,纵坐标为溶液的pH。下列说法正确的是( )
A.此一元弱酸的电离常数(Ka)约为1.0×10-6
B.此弱酸的浓度为1×10-4mol/L
C.此实验可选用甲基橙作指示剂
D.此实验可选用酚酞作指示剂
【答案】AD
【解析】
由图像可知,V=10mL时,恰好中和,该弱酸电离程度近似1%,所以弱酸起始浓度为1×10-2mol/L,电离常数Ka约为10-4×10-4/10-2=
1.0×10-6,A正确,B错误;当恰好中和中和时为强碱弱酸盐,水解显碱性,应选择酚酞,C错误,D正确;故答案为:AD。

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
【题目】高炉炼铁过程中发生反应:![]() ,该反应在不同温度下的平衡常数见表。下列说法正确的是( )
,该反应在不同温度下的平衡常数见表。下列说法正确的是( )
温度T/℃ | 1000 | 1150 | 1300 |
平衡常数K | 4.0 | 3.7 | 3.5 |
A.平衡后温度不变缩小容器容积,![]() 的转化率升高
的转化率升高
B.增加高炉的高度可以有效降低炼铁尾气中CO的含量
C.其他条件不变时,增大c(CO),该反应的K值增大
D.由表中数据可判断该反应:反应物总能量大于生成物的总能量