题目内容
(10分)有X、Y、Z三种短周期元素,X的气态氢化物化学式为H2X,此氢化物的分子量与X最高价氧化物的分子量之比为17:40,X原子核内质子数与中子数相等,Y与X可以形成离子化合物Y2X,Y的阳离子电子层结构与Ne相同,Z与X同周期,其气态单质是双原子分子,两原子共用1对电子。试回答:
(1)写出各元素符号:X 、Y 、Z 。
(2)X离子的结构示意图为 。X与Y形成的离子化合物的电子式为 , Z和氢形成的化合物的电子式为 。
(3)Y单质在空气中燃烧的化学方程式为 ,生成物与水反应的化学方程式为 。
(1)S,Na,Cl
(2)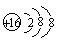 ,
,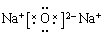 ,
, 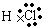
(3)2Na + O2 Na2O2,2Na2O2 + 2H2O =" 4NaOH" + O2↑。
Na2O2,2Na2O2 + 2H2O =" 4NaOH" + O2↑。
解析试题分析:短周期元素,X的气态氢化物化学式为H2X,此氢化物的分子量与X最高价氧化物的分子量之比为17:40。则X是S;Y与X可以形成离子化合物Y2X,Y的阳离子电子层结构与Ne相同,则Y是Na;Z与X同周期,其气态单质是双原子分子,两原子共用1对电子。则Z是Cl.(1)X是S;Y是Na;Z是Cl。(2)S2-的结构示意图为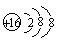 ,Na与S形成的化合物Na2S的电子式为
,Na与S形成的化合物Na2S的电子式为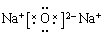 。H、Cl形成的化合物HCl的电子式为:
。H、Cl形成的化合物HCl的电子式为: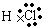 。(3)Na在空气中燃烧的方程式为2Na + O2
。(3)Na在空气中燃烧的方程式为2Na + O2 Na2O2;生成物Na2O2与水反应的化学方程式为2Na2O2 + 2H2O =" 4NaOH" + O2↑。
Na2O2;生成物Na2O2与水反应的化学方程式为2Na2O2 + 2H2O =" 4NaOH" + O2↑。
考点:考查元素的推断及原子结构示意图、离子化合物、共价化合物的电子式表示、方向方程式的书写。

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式回答以下问题:
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | | | | | ① | | ② | |
| 三 | ③ | ④ | ⑤ | ⑥ | | | ⑦ | ⑧ |
| 四 | ⑨ | | | | | | ⑩ | |
(1)在这些元素中,金属性最强的元素是
(2)化学性质最不活泼的元素其原子结构示意图为 ;
(3)元素的最高价氧化物对应的水化物中酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 ;
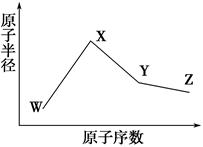
(4)在③~⑦元素中,原子半径最大的是 ,原子半径最小的是 ;
(5)在⑦与⑩的单质中,化学性质较活泼的是 ,可用什么化学反应说明该事实(写出反应的化学方程式): 。

 Si3N4(s) + 12HCl(g) △H<0
Si3N4(s) + 12HCl(g) △H<0