题目内容
18.下列说法不正确的是( )| A. | 离子化合物中一定只含离子键 | |
| B. | 共价化合物中一定只含共价键 | |
| C. | 离子化合物中不一定含有金属元素 | |
| D. | 共价键不一定只存在于共价化合物中 |
分析 含有离子键的化合物属于离子化合物,离子化合物中可能含有共价键;只含有共价键的化合物属于共价化合物,共价化合物中一定没有离子键,以此解答该题.
解答 解:A.离子化合物中肯定含有离子键,可能含共价键,如NaOH,故A错误;
B.共价化合物只含有共价键,离子键只存在于离子化合物中,故B正确;
C.铵盐为离子化合物,但由非金属元素组成,故C正确;
D.共价键可存在非金属单质或共价化合物中,故D正确.
故选A.
点评 本题考查了离子键、共价键与离子化合物、共价化合物的关系,侧重考查学生对这几个概念的辨别能力,要注意离子化合物中可能含共价键,共价化合物中一定不含离子键.

练习册系列答案
相关题目
3.我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇.则下列说法正确的是( )
| A. | 乙醇分子中的官能团是酚羟基 | |
| B. | 使用K2Cr2O7酸性溶液检测酒驾,是利用了乙醇的氧化性 | |
| C. | 乙醇可以发生取代、消去和氧化反应 | |
| D. | 将75%的乙醇与98%的浓硫酸混合液迅速加热至170°C以制取乙烯 |
9.下列溶液中微粒的物质的量浓度关系不正确的是( )
| A. | 将10ml0.1mol•L-1Na2CO3溶液逐滴滴加到10ml0.1mol•L-1盐酸中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-) | |
| B. | 若将CO2 通入0.1 mol•L-1Na2CO3溶液中至溶液中性,则溶液中2 c(CO32ˉ)+c(HCO3ˉ)=0.1 mol•L-1 | |
| C. | 常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为碱性 | |
| D. | 等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数大小:N前<N后 |
13.有机物分子间或原子与原子团间的相互影响会导致物质化学物质的不同,下列各项的事实不能说明上述观点的是( )
| A. | 乙烯能发生加成反应,而乙烷不能发生加成反应 | |
| B. | 甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 | |
| C. | 苯与硝酸在加热的条件下发生取代反应,而甲苯在常温下就能与硝酸发生反应 | |
| D. | 酚和醇的羟基性质差别较大 |
3.已知:
①H2O(g)═H2O(l)△H=-Q1kJ.mol-1
②C2H5OH(g)═C2H5OH(1)△H=-Q2kJ.mol-1
③C2H5OH(g)═302(g)=2C02(g)+3H20(g)△H=-Q3 kJ.mol-1
下列判断正确的是( )
①H2O(g)═H2O(l)△H=-Q1kJ.mol-1
②C2H5OH(g)═C2H5OH(1)△H=-Q2kJ.mol-1
③C2H5OH(g)═302(g)=2C02(g)+3H20(g)△H=-Q3 kJ.mol-1
下列判断正确的是( )
| A. | 酒精的燃烧热AH=-Q3 kJ•mol-1 | |
| B. | 由③可知1molC2H5OH(g)的能量高于2molC02(g)和3 molH20(g)的总能量 | |
| C. | H20(g)→H20( 1)释放出了热量,所以该过程为放热反应 | |
| D. | 23g液体酒精完全燃烧生成C02(g)和H20( 1),释放热量为(0.5Q3-0.5Q2+1.5Q1)kJ |
10.下列化学用语书写正确的是( )
| A. | 乙炔的最简式:CHCH | B. | 甲基苯的官能团为: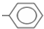 | ||
| C. | 丙烷分子的球棍模型示意图: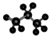 | D. | -CH3(甲基)的电子式为: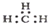 |
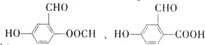 .
.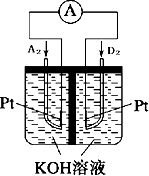 A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答:
A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答: .
. .
. 为了验证铜与稀硝酸反应产生的是一氧化氮而不是氢气.某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;C中有足量的澄清石灰水,E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
为了验证铜与稀硝酸反应产生的是一氧化氮而不是氢气.某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;C中有足量的澄清石灰水,E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.