题目内容
19.0.3mol的氧气和0.2mol的臭氧(O3):(1)它们的质量比1:1,
(2)它们所含的分子数比3:2,
(3)它们所含的原子数比1:1,
(4)它们同温同压时的体积比是3:2.
分析 (1)根据m=n•M计算质量,然后作比较;
(2)根据N=n•NA分子数目之比等于其物质的量之比;
(3)氧气含有氧原子为氧气分子2倍,臭氧含有氧原子数目为臭氧3倍,据此计算含有氧原子数目之比;
(4)根据V=n•Vm可知,相同条件下气体体积之比等于其物质的量之比.
解答 解:(1)根据m=n•M可知,0.3mol的氧气和0.2mol的臭氧(O3)的质量之比为:0.3mol×32g/mol:0.2mol×48g/mol=1:1,
故答案为:1:1;
(2)根据N=n•NA可知,二者含有分子数目之比为0.3mol:0.2mol=3:2,
故答案为:3:2;
(3)氧气含有氧原子为氧气分子2倍,臭氧含有氧原子数目为臭氧3倍,二者含有分子数目之比为3:2,含有氧原子数目之比为3×2:2×3=1:1,
故答案为:1:1;
(4)根据V=n•Vm可知,相同条件下气体体积之比等于其物质的量之比,故二者体积之比为0.3mol:0.2mol=3:2,
故答案为:3:2.
点评 本题考查物质的量有关计算,比较基础,难度不大,注意对公式的理解与灵活应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.下列反应中,水只作氧化剂的是( )
| A. | Cl2+H2O═HCl+HClO | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | 2Na+2H2O═4NaOH+H2↑ | D. | 2H2O═2H2↑+O2↑ |
7.工业上铁的冶炼是在炼铁高炉中进行的,发生的反应是 Fe2O3+3CO═2Fe+3CO2,此反应属于( )
| A. | 化合反应 | B. | 氧化还原反应 | C. | 置换反应 | D. | 分解反应 |
4.(1)在25℃、101kPa下,1g乙烷燃烧生成CO2和液态水时放热QkJ.则表示乙烷燃烧热的热化学方程式为C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-30QkJ/mol.
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ•mol-1):
根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)═CF4(g)+4HF(g)△H=-1928kJ/mol.
(3)下列说法不正确的是(填序号)AD
A.某温度下纯水中的C(H+)=10-6,故其显酸性
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
C.相同温度下,0.1mol•L-1NH4Cl溶液中NH4+的浓度比0.1mol•L-1氨水中NH4+的浓度大;
D.相同温度下,PH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度大;
E.向饱和石灰水中加入CaO固体,溶液中Ca2+、OH-的物质的量均减小.
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ•mol-1):
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
CH4(g)+4F2(g)═CF4(g)+4HF(g)△H=-1928kJ/mol.
(3)下列说法不正确的是(填序号)AD
A.某温度下纯水中的C(H+)=10-6,故其显酸性
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
C.相同温度下,0.1mol•L-1NH4Cl溶液中NH4+的浓度比0.1mol•L-1氨水中NH4+的浓度大;
D.相同温度下,PH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度大;
E.向饱和石灰水中加入CaO固体,溶液中Ca2+、OH-的物质的量均减小.
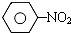 $\stackrel{Fe、HCl、H_{2}O}{→}$
$\stackrel{Fe、HCl、H_{2}O}{→}$
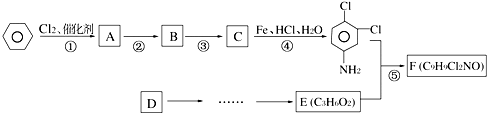
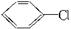 .反应②条件为浓硫酸加热.
.反应②条件为浓硫酸加热.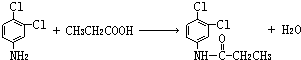 ;该反应的反应类型为取代反应.
;该反应的反应类型为取代反应.
 实验室欲配制980mL0.100mol•L-1Na2CO3溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平
实验室欲配制980mL0.100mol•L-1Na2CO3溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平