题目内容
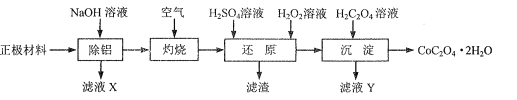
【题目】2019年诺贝尔化学奖授予锂离子电池的发明者,锂离子电池是目前应用广泛的一类电池。以钛铁矿(主要成分为FeTiO3,含有少量MgO、Fe2O3、SiO2等杂质)为原料,制备锂离子电池电极材料的工艺流程如图所示:
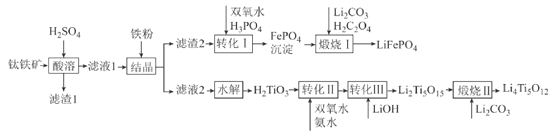
已知:①滤液1中含Ti微粒的主要存在形式为TiO2+;
②)Ksp(FePO4)=1.3×10-22、Ksp[Mg3(PO4)2]=1.0×10-24;溶液中某离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全。
请回答下列问题:
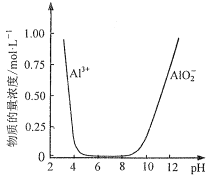
(1)滤渣1中主要成分的化学式为__。
(2)“结晶”温度需控制在70℃左右,若温度过高会导致的后果为__。
(3)“转化I”后所得溶液中c(Mg2+)=0.01mol·L-1,若其中Fe3+沉淀完全,则溶液中c(PO43-)的范围为__。
(4)“煅烧I”反应中氧化剂和还原剂的物质的量之比为__。
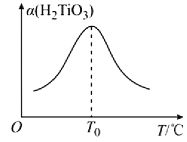
(5)“转化II”中H2TiO3的转化率(α)与温度(T)的关系如图所示。T0℃时,一定时间内H2TiO3的转化率最高的原因为__。
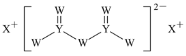
(6)Li2Ti5O15中-1价与-2价O原子的数目之比为___。“煅烧II”反应中同时生成两种参与大气循环的气体,该反应的化学方程式为__。
(7)某锂离子电池放电时的电池反应为Li1-xFePO4+LixC6=LiFePO4+6C,则充电时阳极的电极反应式为__。
【答案】SiO2 TiO2+会提前水解而降低H2TiO3的产率,且使滤渣2中混有杂质 ![]() mol/L
mol/L ![]() c(PO43-)<1.0
c(PO43-)<1.0![]() 10-9mol/L 2:1 温度低于T0℃时,反应速率随温度升高而加快,H2TiO3的转化率升高,高于T0℃时后,双氧水分解和氨气的挥发导致反应速率减小,使H2TiO3的转化率降低 8:7 Li2Ti5O15+Li2CO3
10-9mol/L 2:1 温度低于T0℃时,反应速率随温度升高而加快,H2TiO3的转化率升高,高于T0℃时后,双氧水分解和氨气的挥发导致反应速率减小,使H2TiO3的转化率降低 8:7 Li2Ti5O15+Li2CO3![]() Li4Ti5O12+2O2
Li4Ti5O12+2O2![]() +CO2
+CO2![]() LiFePO4-xe-= Li1-xFePO4+xLi+
LiFePO4-xe-= Li1-xFePO4+xLi+
【解析】
铁矿石加入硫酸溶解过滤得到滤渣为二氧化硅,滤液1为MgCl2、FeCl3、TiOSO4,加铁粉与过量硫酸反应并调pH,滤液中TiO2+水解得到H2TiO3,加入过氧化氢和氨水、氢氧化锂溶液得到沉淀Li2Ti5O15,加入碳酸锂煅烧得到钛酸锂Li4Ti5O12,滤渣2加入过氧化氢氧化亚铁离子,加入磷酸得到沉淀磷酸铁,加入碳酸锂和草酸煅烧得到磷酸亚铁锂LiFePO4;据此分析解答。
(1)钛铁矿的成分中只有SiO2不溶于硫酸,滤渣1的成分为SiO2,故答案为:SiO2;
(2)“结晶”温度需控制在70℃左右,如果温度过高,TiO2+会提前水解而降低H2TiO3的产率,且使滤渣2中混有杂质,故答案为:TiO2+会提前水解而降低H2TiO3的产率,且使滤渣2中混有杂质;
(3)Fe3+刚好沉淀完全时,c(PO43-)=![]() =
=![]() mol/L,要保证Fe3+沉淀完全,c(PO43-)应该
mol/L,要保证Fe3+沉淀完全,c(PO43-)应该![]()
![]() mol/L;c(Mg2+)=0.01mol·L-1,若刚好产生沉淀,c(PO43-)=
mol/L;c(Mg2+)=0.01mol·L-1,若刚好产生沉淀,c(PO43-)=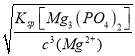 =
=![]() =1.0
=1.0![]() 10-9mol/L,而按题意分析应不能使镁离子沉淀,故c(PO43-)<1.0
10-9mol/L,而按题意分析应不能使镁离子沉淀,故c(PO43-)<1.0![]() 10-9mol/L,故答案为:
10-9mol/L,故答案为:![]() mol/L
mol/L ![]() c(PO4span>3-)<1.0
c(PO4span>3-)<1.0![]() 10-9mol/L;
10-9mol/L;
(4)“煅烧I”反应中氧化剂为FePO4,反应后被还原为LiFePO4,1mol氧化剂得到1mol电子;还原剂为H2C2O4,被氧化成CO2,1mol还原剂失去2mol电子,根据电子守恒,氧化剂与还原剂的物质的量比值为:2:1,故答案为:2:1;
(5)“转化II”中H2TiO3的转化率(α)与温度(T)的关系如图所示,温度低于T0℃时,反应速率随温度升高而加快,H2TiO3的转化率升高,高于T0℃时后,双氧水分解和氨气的挥发导致反应速率减小,使H2TiO3的转化率降低,所以T0℃时,一定时间内H2TiO3的转化率最高,故答案为:温度低于T0℃时,反应速率随温度升高而加快,H2TiO3的转化率升高,高于T0℃时后,双氧水分解和氨气的挥发导致反应速率减小,使H2TiO3的转化率降低;
(6)Li2Ti5O15中Li显+1价,Ti显+4价,根据代数和为零可算出15个O共显-22价,设-1价O数目为x,-2价O数目为y,有x+y=15;-x-2y=-22,算出x=8,y=7,-1价与-2价O原子的数目之比为8:7;“煅烧II”反应中同时生成的两种参与大气循环的气体应为O2和CO2,可写出化学方程式为:Li2Ti5O15+Li2CO3![]() Li4Ti5O12+2O2
Li4Ti5O12+2O2![]() +CO2
+CO2![]() ;故答案为:8:7;Li2Ti5O15+Li2CO3
;故答案为:8:7;Li2Ti5O15+Li2CO3![]() Li4Ti5O12+2O2
Li4Ti5O12+2O2![]() +CO2
+CO2![]() ;
;
(7)电池反应为Li1-xFePO4+LixC6=LiFePO4+6C,LixC6为负极,Li1-xFePO4为正极,充电时阳极反应应该是LiFePO4变为Li1-xFePO4,电极反应式为:LiFePO4-xe-= Li1-xFePO4+xLi+,故答案为:LiFePO4-xe-= Li1-xFePO4+xLi+。