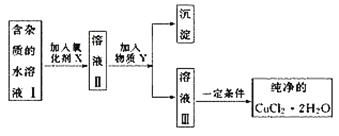
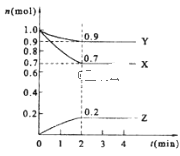
题目内容
【题目】叠氮酸(HN3)与醋酸的酸性相似,0.2 mol HN3与0.2 mol NaOH反应后将溶液稀释至500 mL,测得溶液pH=a,下列说法一定错误的是( )
A.HN3水溶液中微粒浓度大小顺序为c(HN3)>c(H+)>c(N3—)>c(OH-)
B.题示500 mL溶液中离子浓度大小顺序为c(Na+)>c(N3—)>c(OH-)>c(H+)
C.题示500 mL溶液中由水电离产生的c(OH-)=1×10-amol·L-1
D.根据题给数据可以计算该温度下叠氮酸的电离平衡常数Ka
【答案】C
【解析】
A. 叠氮酸与醋酸的酸性相似,则叠氮酸是弱酸,其电离程度很小,水溶液中叠氮酸和水都电离生成氢离子,只有HN3电离生成N3,所以离子浓度大小顺序是c(HN3)>c(H+)>c(N3—)>c(OH-),故A正确;
B. 强碱弱酸盐NaN3水解导致溶液显碱性,离子浓度大小顺序为c(Na+)>c(N3-)>c(OH)>c(H+),故B正确;
C. 强碱弱酸盐NaN3水解,溶液pH=α,c(H+)=1×10αmolL1,由水电离产生的c(OH)=1×10(14a)molL1,故C错误;
D. 据溶液pH和水的离子积常数可以求得氢离子和氢氧根离子浓度,因为叠氮酸根离子的水解,叠氮酸分子浓度为氢氧根离子浓度与氢离子浓度差,钠离子浓度不变,为![]() =0.4mol/L,据电荷守恒,c(Na+)+c(H+)=c(N3)+c(OH)可以求得叠氮酸根离子浓度,进而求得Ka,故D正确;
=0.4mol/L,据电荷守恒,c(Na+)+c(H+)=c(N3)+c(OH)可以求得叠氮酸根离子浓度,进而求得Ka,故D正确;
故选C。

 考前必练系列答案
考前必练系列答案【题目】已知:H2(g)+I2(g) ![]() 2HI(g) H=-149kJ/mol。在甲、乙两个体积相同的密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。
2HI(g) H=-149kJ/mol。在甲、乙两个体积相同的密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。
起始 浓度 | c(H2)(mol/L) | c(I2)(mol/L) | c(HI)/(mol/L) |
甲 | 0.01 | 0.01 | 0 |
乙 | 0.02 | 0.02 | 0 |
甲中反应达到平衡时,测得c(H2)=0.008 mol/L下列判断正确的是( )
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25
【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) ![]() 2G(g)。平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。平衡时G的体积分数(%)随温度和压强的变化如下表所示:
温度/体积分数/压强 | 1.0 | 2.0 | 3.0 |
810 | 54.0 | a | B |
915 | c | 75.0 | D |
1000 | E | f | 83.0 |
①b<f ②915 ℃、2.0 MPa时E的转化率为60% ③该反应的ΔS>0 ④K(1 000 ℃)>K(810 ℃) 上述①~④中正确的 ( )
A.①②B.②③C.②③④D.①②③④
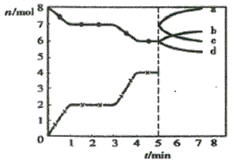
【题目】800°C时,在2L密闭容器中发生反应2NO(g)+O2(g)![]() 2NO2(g) H<0,测得n(NO)随时间的变化如下表:
2NO2(g) H<0,测得n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)NO的平衡浓度c(NO)=____________________。
(2)下图中表示NO2的变化的曲线______________。(填字母)
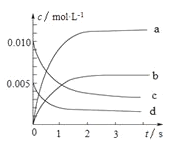
(3)能说明该反应已经达到化学平衡状态的是______________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=v正(O2) D.容器内NO、O2、NO2同时存在
(4)下列操作中,能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
A.及时分离出NO2气体B.适当升高温度
C.增大O2的浓度D.选择高效的催化剂
(5)下图中的曲线表示的是其它条件一定时,体系中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示v(正)<v(逆)的点是____________。(填选项)
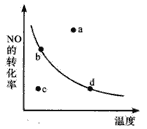
A.a B.b C.c D.d
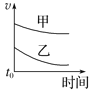
【题目】下列表格中的各种情况,可以用对应选项中的图像表示的是
选项 | 反应 | 甲 | 乙 |
A | 外形、大小相近的金属和水反应 | Na | K |
B | 4mL0.01mol·L-1 KMnO4溶液分别和不同浓度的2mLH2C2O4(草酸)溶液反应 | 0.1mol·L-1的H2C2O4溶液 | 0.2mol·L-1的H2C2O4溶液 |
C | 5mL0.1mol·L-1Na2S2O3溶液和5mL0.1mol·L-1H2SO4溶液反应 | 热水 | 冷水 |
D | 5mL4%的过氧化氢溶液分解放出O2 | 无MnO2粉末 | 加MnO2粉末 |
A.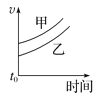 B.
B.
C. D.
D.