题目内容
【题目】(1)现有下列十种物质:①蔗糖②熔融NaCl③石墨④铜丝⑤NaOH固体⑥SO2⑦NaHSO4固体⑧K2O固体⑨液态H2SO4⑩饱和FeCl3溶液 上述物质中可导电的是________(填序号,下同);上述物质中不能导电,但属于电解质的是_______________________。
(2)NaHSO4是一种酸式盐,请填写下列空白:
①NaHSO4晶体熔化时的电离方程式为______________________________。
②3 mol·L-1 NaHSO4与2 mol·L-1 Ba(OH)2溶液等体积混合,该反应总的离子方程为___________。
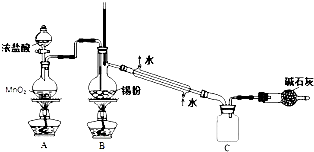
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为________________________________________________。
(4)某强酸性反应体系中,反应物和生成物共六种物质:O2、MnO4-、H2O、Mn2+、H2O2、H+,已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式:_________________________。
【答案】 ②③④⑩ ⑤⑦⑧⑨ NaHSO4(熔融) =Na++ HSO4- 3H++2SO42-+2Ba2++3OH-=2BaSO4↓+3H2O ⑩ Fe3+ +3H2O ![]() Fe(OH)3(胶体) +3H+ 5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8 H2O
Fe(OH)3(胶体) +3H+ 5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8 H2O
【解析】(1)①蔗糖非电解质,不导电;②熔融的NaCl是电解质,能导电;③石墨能导电;④铜丝能导电;⑤NaOH固体不导电,但是电解质;⑥SO2是非电解质,不导电;⑦NaHSO4固体不导电,但是电解质;⑧K2O固体不导电,但是电解质;⑨液态H2SO4不导电,但是电解质;⑩饱和FeCl3溶液能导电,但既不是电解质也不是非电解质;因此能导电的是②③④⑩,属于电解质的是⑤⑦⑧⑨;
(2)①NaHSO4晶体熔化时的电离方程式为:NaHSO4(熔融)=Na++HSO4-;②3 molL-1 NaHSO4与2 molL-1 Ba(OH)2溶液等体积混合时,Ba2+完全转化为沉淀,H+反应完全,该反应总的离子方程式为3H++2SO42-+2Ba2++3OH-=2BaSO4↓+3H2O;
(3)制备氢氧化铁胶体的方法是向沸水中低价饱和的FeCl3溶液,所以选⑩,离子方程式为:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+;
Fe(OH)3(胶体)+3H+;
(4)根据以上分析,依据电子得失总数相等配平离子方程式为:5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8 H2O

 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案【题目】某市对大气进行监测,发现该市首要污染物可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此PM2.5、SO2、NO2等你进行研究具有重要意义.请回答下列问题:
(1)对PM2.5样本用适量蒸馏水处理制成待测试样.测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 | K+ | Na+ | NH4+ | SO42﹣ | NO3﹣ | Cl﹣ |
浓度/molL﹣1 | 4×10﹣6 | 6×10﹣4 | 2×10﹣5 | 4×10﹣5 | 3×10﹣5 | 2×10﹣5 |
根据表中数据判断PM2.5的酸碱性为 , 试样的PH值= .
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.
已知:H2(g)+ ![]() O2(g)=H2O(g)△H=﹣241.8kJ/mol﹣1
O2(g)=H2O(g)△H=﹣241.8kJ/mol﹣1
C(s)+ ![]() O2(g)=CO(g)△H=﹣110.5kJ/mol﹣1
O2(g)=CO(g)△H=﹣110.5kJ/mol﹣1
写出焦炭与水蒸气反应的热化学方程式:
②洗涤含SO2的烟气.以下物质可作为洗涤剂的是 .
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化
①已知气缸中生成NO的反应为:N2(g)+O2(g)2NO(g)△H>0.
若1mol空气含0.8mol N2和0.2mol O2 , 1300℃时在密闭容器内反应达到平衡.测得NO的物质的量为8×10﹣4mol,计算该温度下的平衡常数K= . 汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),已知该反应的△H>0,简述该设想能否实现的依据:;
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为 .