题目内容
【题目】一定温度下,水溶液中H+和OH﹣的浓度变化曲线如图,下列说法正确的是( ) 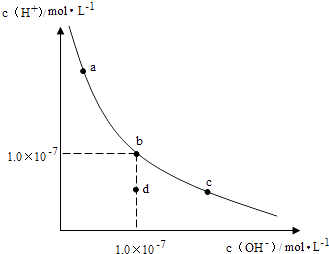
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10﹣13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
【答案】C
【解析】解:A、由图可知abc三点对应的平衡常数不变,故abc为等温线,故升高温度,不能由c到b,故A错误; B、b点c(H+)=c(OH﹣)=1.0×10﹣7 , 故KW=1.0×10﹣7×1.0×10﹣7=1.0×10﹣14 , 故B错误;
C、加入FeCl3 , 氯化铁为强酸弱碱盐,铁离子结合水电离出的氢氧根,促进水的电离平衡右移,即氢离子浓度增大,氢氧根离子浓度减小(由b到a),符合图象变化趋势,故C正确;
D、由c点到d点,水的离子积常数减小,温度不变,K不变,故不能利用稀释使其形成此变化,故D错误,
故选C.
A、由图可知abc为等温线;
B、由b点计算此温度下水的离子积常数为1.0×10﹣14;
C、b点到a点,氢离子浓度变大,氢氧根离子浓度减小,据此解答即可;
D、稀释不会引起水的离子积的改变,据此解答即可.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目