题目内容
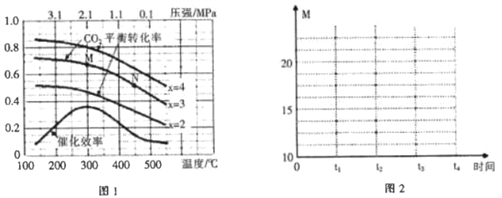
【题目】NO和CO2的混合气体,通过过量的Na2O2后,剩余气体体积为原来的一半,则NO和CO2的体积比为(不考虑NOx与Na2O2的反应及2NO2![]() N2O4)( )
N2O4)( )
A. 2:1 B. 1:2 C. 1:4 D. ≤1:1的任意比
【答案】D
【解析】
设NO和CO2的体积分别为x、y,则根据方程式可知
2CO2+2Na2O2=2Na2CO3+O2 △V
2 1 1
y 0.5y
2NO+O2=2NO2 △V
2 1 2 1
x 0.5x
显然x=y时满足剩余气体体积为原来的一半,若x>y时,剩余气体体积大于原来的一半,若x<y时满足剩余气体体积为原来的一半,综上所述,剩余气体体积为原来的一半,NO和CO2的体积比为≤1:1的任意比,故答案选D。

 互动英语系列答案
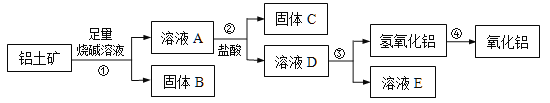
互动英语系列答案【题目】某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾大晶体,具体流程如下:

已知:AlCl3·6H2O易溶于水、乙醇及乙醚;明矾在水中的溶解度如下表。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
请回答:
(1)步骤Ⅰ中的化学方程式_________;步骤Ⅱ中生成Al(OH)3的离子方程式___________。
(2)步骤Ⅲ,下列操作合理的是____________。
A.坩埚洗净后,无需擦干,即可加入Al(OH)3灼烧
B.为了得到纯Al2O3,需灼烧至恒重
C.若用坩埚钳移动灼热的坩埚,需预热坩埚钳
D.坩埚取下后放在石棉网上冷却待用
E.为确保称量准确,灼烧后应趁热称重
(3)步骤Ⅳ,选出在培养规则明矾大晶体过程中合理的操作并排序_______________。
①迅速降至室温 ②用玻璃棒摩擦器壁 ③配制90℃的明矾饱和溶液 ④自然冷却至室温 ⑤选规则明矾小晶体并悬挂在溶液中央 ⑥配制高于室温10-20℃的明矾饱和溶液
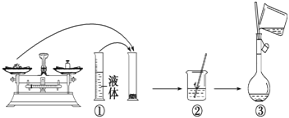
(4)由溶液A制备AlCl3·6H2O的装置如下图:

①通入HCl的作用是抑制AlCl3水解和________________________。
②步骤Ⅴ,抽滤时,用玻璃纤维替代滤纸的理由是_____;洗涤时,合适的洗涤剂是_____。
③步骤Ⅵ,为得到纯净的AlCl3·6H2O,宜采用的干燥方式是______________。