题目内容
下列说法正确的是( )
| A、7.8克Na2S和Na2O2的固体混合物中含有的阴离子数目为0.1NA | ||||
B、用铜做电极电解CuSO4溶液的反应方程式:2Cu2++2H2O
| ||||
| C、常温时,浓度均为0.01mol/L的Na2CO3溶液和NaHCO3溶液等体积混合,其溶液中粒子浓度关系为c(CO32-)+c(HCO3-)+c(H2CO3)=0.02mol/L | ||||
| D、在蒸馏水中滴加浓H2SO4,KW不变 |
考点:不同晶体的结构微粒及微粒间作用力的区别,水的电离,电解原理,离子浓度大小的比较
专题:基本概念与基本理论
分析:A.计算物质的量,结合离子晶体的构成判断;
B.阳极铜被氧化,不能生成氧气;
C.根据物料守恒判断;
D.浓硫酸溶于水放热.
B.阳极铜被氧化,不能生成氧气;
C.根据物料守恒判断;
D.浓硫酸溶于水放热.
解答:
解:A.Na2S和Na2O2的摩尔质量相同,7.8克Na2S和Na2O2的固体的物质的量为0.1mol,Na2O2的固体中阴离子为O22-,则阴离子数目为0.1NA,故A正确;
B.阳极铜被氧化,不能生成氧气,为铜的精炼,阳极铜被氧化,阴极析出铜,故B错误;
C.浓度均为0.01mol/L的Na2CO3溶液和NaHCO3溶液等体积混合,其溶液中粒子浓度关系为c(CO32-)+c(HCO3-)+c(H2CO3)=0.01mol/L,故C错误;
D.浓硫酸溶于水放热,KW增大,故D错误.
故选A.
B.阳极铜被氧化,不能生成氧气,为铜的精炼,阳极铜被氧化,阴极析出铜,故B错误;
C.浓度均为0.01mol/L的Na2CO3溶液和NaHCO3溶液等体积混合,其溶液中粒子浓度关系为c(CO32-)+c(HCO3-)+c(H2CO3)=0.01mol/L,故C错误;
D.浓硫酸溶于水放热,KW增大,故D错误.
故选A.
点评:本题考查较为综合,涉及晶体、电解、水解以及水的电离等问题,为高考常见题型,侧重于学生的分析能力的考查,注意相关基础知识的积累,易错点为C,注意物料守恒的运用,难度中等.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
关于氮的变化关系图如下:
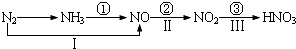
则下列说法正确的是( )

则下列说法正确的是( )
| A、路线①②③是工业生产硝酸的主要途径 |
| B、路线ⅠⅡⅢ是雷电固氮生成硝酸的主要途径 |
| C、上述并不是所有反应都是氧化还原反应 |
| D、上述反应中①②③均属于氮的固定 |
下列离子方程式正确的是( )
| A、氢硫酸与CuSO4溶液混合:S2-+Cu2+═CuS↓ | ||||
| B、磷酸二氢钙溶液跟足量NaOH溶液反应:3Ca2++2H2PO4-+4OH-═Ca3(PO4)2↓+4H2O | ||||
| C、硝酸亚铁溶液中滴入稀硫酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O | ||||
D、电解MgCl2溶液:2H2O+2Cl-
|
下列各组物质中性质的变化规律排列正确的是( )
| A、微粒半径:Al3+>Mg2+>Na+>F- |
| B、稳定性:HI>HBr>HCl>HF |
| C、酸性:HClO4>H2SO4>H3PO4>H4SiO4 |
| D、碱性:Ca(OH)2>KOH>Mg(OH)2>Al(OH)3 |
下列关于元素周期表的说法正确的是( )
| A、能生成碱的金属元素都在ⅠA族 |
| B、第 IA族元素金属性强于第ⅡA族元素 |
| C、稀有气体元素原子的最外层电子数均为8 |
| D、第二周期ⅣA族元素的原子中子数不一定为6 |
下列不能使淀粉碘化钾试纸变蓝的物质是( )
| A、碘水 | B、溴水 |
| C、氯水 | D、溴化钠溶液 |
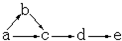 a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:
a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化: