题目内容
关于氮的变化关系图如下:
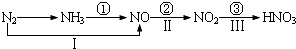
则下列说法正确的是( )

则下列说法正确的是( )
| A、路线①②③是工业生产硝酸的主要途径 |
| B、路线ⅠⅡⅢ是雷电固氮生成硝酸的主要途径 |
| C、上述并不是所有反应都是氧化还原反应 |
| D、上述反应中①②③均属于氮的固定 |
考点:氮族元素简介
专题:氮族元素
分析:A.工业上生产硝酸的流程是:氮气和氢气生成氨气,氨气与氧气反应生成一氧化氮和水,一氧化氮与氧气反应生成二氧化氮、二氧化氮被水吸收生成硝酸和一氧化氮;
B.自然雷电固氮原理是,在放电条件下,氮气和氧气生成一氧化氮,一氧化氮性质不稳定,迅速被空气中的氧气氧化为二氧化氮,二氧化氮溶于水生成硝酸;
C.氧化还原反应的特征是化合价的升降,可从元素的化合价是否发生变化的角度判断是否属于氧化还原反应;
D.氮的固定是指空气中游离态的氮转化为化合态的氮的过程;
B.自然雷电固氮原理是,在放电条件下,氮气和氧气生成一氧化氮,一氧化氮性质不稳定,迅速被空气中的氧气氧化为二氧化氮,二氧化氮溶于水生成硝酸;
C.氧化还原反应的特征是化合价的升降,可从元素的化合价是否发生变化的角度判断是否属于氧化还原反应;
D.氮的固定是指空气中游离态的氮转化为化合态的氮的过程;
解答:
解:A.工业上生产硝酸的流程是:氮气和氢气生成氨气,氨气与氧气反应4NH3+5O2
4NO+6H2O路线①,一氧化氮与氧气反应2NO+O2=2NO2 路线②,二氧化氮被水吸收3NO2+H2O═2HNO3+NO路线③,路线①②③是工业生产硝酸的主要途径,故A正确;
B.在放电条件下,氮气和氧气发生化合反应:N2+O2
2NO路线Ⅰ;NO不稳定,易被氧气氧化为二氧化氮:2NO+O2═2NO2路线Ⅱ,二氧化氮溶于水生成硝酸:3NO2+H2O═2HNO3+NO路线Ⅲ,故B正确;
C.从氮的变化关系图可知:N从N2(0价)→NO(+2价)→NO2(+5价)→HNO3(+5价),都是氧化还原反应,故C错误;
D.上述反应中①空气中的氮气转变为含氮化合物,符合氮的固定的定义,属于氮的固定,②③含氮化合物转变为其它物质,是氮的化合物之间的转化,不是氮的固定,故D错误;
故选AB.
| ||
| △ |
B.在放电条件下,氮气和氧气发生化合反应:N2+O2
| ||
C.从氮的变化关系图可知:N从N2(0价)→NO(+2价)→NO2(+5价)→HNO3(+5价),都是氧化还原反应,故C错误;
D.上述反应中①空气中的氮气转变为含氮化合物,符合氮的固定的定义,属于氮的固定,②③含氮化合物转变为其它物质,是氮的化合物之间的转化,不是氮的固定,故D错误;
故选AB.
点评:本题考查了氮及其化合物的转变关系,掌握工业上生产硝酸、雷电固氮的原理是解答的关键,注意对氮的固定的概念的掌握,题目难度中等.

练习册系列答案
相关题目
质量相同的下列醇分别与过量的钠作用放出氢气最多的是( )
| A、甲醇 | B、乙醇 |
| C、乙二醇 | D、丙三醇 |
下列叙述或操作不正确的是( )
| A、浓硫酸具有强氧化性,稀硫酸无氧化性 |
| B、浓硫酸不慎沾到皮肤上,立即用大量的水冲洗 |
| C、稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌 |
| D、浓硫酸与碳的反应中,浓硫酸仅表现强氧化性 |
下列金属中不属于货币金属的是( )
| A、铁 | B、金 | C、银 | D、铜 |
下列说法正确的是( )
| A、7.8克Na2S和Na2O2的固体混合物中含有的阴离子数目为0.1NA | ||||
B、用铜做电极电解CuSO4溶液的反应方程式:2Cu2++2H2O
| ||||
| C、常温时,浓度均为0.01mol/L的Na2CO3溶液和NaHCO3溶液等体积混合,其溶液中粒子浓度关系为c(CO32-)+c(HCO3-)+c(H2CO3)=0.02mol/L | ||||
| D、在蒸馏水中滴加浓H2SO4,KW不变 |
化学与生产、生活、科技等密切相关,下列说法正确的是( )
| A、石油裂解的目的是提高汽油等轻质油的产量和质量 |
| B、“神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 |
| C、高温能杀死流感病毒是因为构成病毒的蛋白质受热变性 |
| D、苯酚稀溶液常用于外科消毒,所以自来水也可以用苯酚进行消毒处理 |
美国科学家成功开发便携式固体氧化物燃料电池,它以丙烷气体为燃料,每填充一次燃料,大约可连续24小时输出50W的电力.一极通人空气,另一极通人丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-,下列对该燃料电池的说法不正确的是( )
| A、在熔融电解质中,O2-由正极移向负极 |
| B、以该电池为电源实现铁上镀银,通入空气的一极与银电极相连 |
| C、通丙烷的电极为电池负极,发生的电极反应为:C3H8-20e-+10O2-=3CO2+4H2O |
| D、电路中每流过5mol电子,必有5.6L丙烷被完全氧化 |